Tioaseton

| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC (preferensi)
Propana-2-tiona[1] | |||
| Nama IUPAC (sistematis)
Tiopropan-2-ona | |||
Nama lain
| |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChemSpider | |||
| Nomor EC | |||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C3H6S | |||
| Massa molar | 74,14 g·mol−1 | ||
| Penampilan | Cairan berwarna oranye hingga coklat | ||
| Bau | Sangat busuk | ||
| Titik lebur | −55 °C (218,15 K / −67 °F)[2] | ||
| Titik didih | 70 °C (343,15 K / 158 °F)[2] | ||
| Bahaya | |||
| Bahaya utama | Bau, iritasi kulit | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
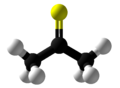
Tioaseton adalah sebuah senyawa organobelerang yang termasuk dalam golongan -tiona yang disebut tioketon, dengan rumus kimia (CH3)2CS. Ia adalah zat oranye atau coklat tak stabil yang dapat diisolasi hanya pada suhu rendah.[3] Di atas suhu −20 °C (−4 °F), tioaseton dapat dengan mudah berubah menjadi polimer dan trimer, tritioaseton.[4] Ia memiliki bau yang sangat kuat dan tak mengenakkan, serta dianggap sebagai salah satu bahan kimia berbau paling buruk yang dikenal manusia.
Tioaseton pertama kali diperoleh pada tahun 1889 oleh Baumann dan Fromm, sebagai pengotor minor dalam sintesis tritioaseton mereka.[2]
Persiapan[sunting | sunting sumber]
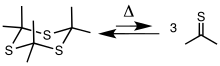
Tioaseton biasanya diperoleh melalui perengkahan trimer siklis tritioaseton, [(CH3)2CS]3. Trimer itu dibuat melalui pirolisis alil isopropil sulfida atau melalui reaksi antara aseton dengan hidrogen sulfida dengan adanya asam Lewis.[5][6] Trimer itu akan merengkah pada suhu 500–600 °C (932–1.112 °F) untuk menghasilkan tiona.[2][7][8]
Polimerisasi[sunting | sunting sumber]
Tidak seperti analog oksigennya aseton, yang tak mudah berpolimerisasi, tioaseton secara spontan akan berpolimerisasi bahkan pada suhu yang sangat rendah, dalam bentuk murni atau yang telah larut dalam eter atau etilena oksida, menghasilkan padatan putih yang merupakan campuran beragam polimer linear ···–[C(CH3)2–S–]n–··· dan trimer siklik tritioaseton. Penyerapan inframerah dari produk ini terjadi terutama pada 2950, 2900, 1440, 1150, 1360, dan 1375 cm−1 karena pasangan metil geminal, serta pada 1085 dan 643 cm−1 karena ikatan C–S. Spektrum NMR 1H menunjukkan puncak tunggal pada x = 8,1.[2]
Berat molekul rata-rata polimer tersebut bervariasi dari 2000 hingga 14000 tergantung pada metode pembuatan, suhu, dan keberadaan tautomer tioenol. Polimer itu melebur dalam kisaran sekitar 70 °C hingga 125 °C. Polimerisasi dipromosikan oleh cahaya dan radikal bebas.[2]
Trimer siklik tioaseton (tritioaseton) adalah senyawa berwarna putih atau nirwarna dengan titik lebur 24 °C (75 °F), mendekati suhu kamar. Ia juga memiliki bau yang tak mengenakkan.[4]
Bau[sunting | sunting sumber]
Tioaseton memiliki bau yang sangat busuk. Seperti banyak senyawa organobelerang dengan berat molekul rendah lainnya, baunya sangat kuat dan dapat dideteksi bahkan ketika sangat encer.[9] Pada tahun 1889, upaya penyulingan bahan kimia di kota Freiburg, Jerman, diikuti oleh kasus mual, muntah-muntah, dan tak sadarkan diri di area dengan radius 0,75 kilometer (0,47 mi) di sekitar laboratorium akibat bau tersebut.[10] Dalam laporan tahun 1890, ahli kimia Inggris di Whitehall Soap Works di Leeds mencatat bahwa pengenceran tampaknya memperburuk bau dan menggambarkan baunya sebagai "menakutkan".[11] Tioaseton dianggap sebagai bahan kimia berbahaya karena baunya yang sangat busuk dan kemampuannya membuat orang tak sadarkan diri, menyebabkan muntah, dan terdeteksi dari jarak jauh.
Pada tahun 1967, peneliti Esso mengulangi percobaan perengkahan tritioaseton, di sebuah laboratorium di selatan Oxford, Britania Raya. Mereka melaporkan pengalaman mereka sebagai berikut:
Baru-baru ini kami menemukan diri kami dengan masalah bau yang melebihi perkiraan terburuk kami. Selama percobaan awal, sebuah sumbat melompat dari residu botol, dan, meskipun diganti sekaligus, mengakibatkan keluhan mual dan sakit segera dari rekan kerja di gedung yang jaraknya 200 yard [180 m]. Dua dari ahli kimia kami yang telah melakukan tak lebih dari menyelidiki perengkahan tritioaseton dalam jumlah kecil mendapati diri mereka menjadi objek tatapan marah di sebuah restoran dan mendapat penghinaan karena pelayan menyemprot area di sekitar mereka dengan pengawabau. Bau tersebut menentang efek pengenceran yang diperkirakan karena pekerja di laboratorium tak menemukan bau yang tak dapat ditoleransi ... dan benar-benar menolak tanggung jawab karena mereka bekerja dalam sistem tertutup. Untuk meyakinkan mereka sebaliknya, mereka dipisahkan dengan pengamat lain di sekitar laboratorium, pada jarak hingga seperempat mil [40 km], dan satu tetes aseton gem-ditiol atau cairan induk dari kristalisasi tritioaseton mentah ditempatkan pada kaca arloji di lemari asap. Baunya kemudian terdeteksi melawan arah angin dalam hitungan detik.[9]
Lihat pula[sunting | sunting sumber]
- Tiobenzofenon, suatu tioketon yang dapat diisolasi sebagai padatan
- Bromoaseton
- Fluoroaseton
- Iodoaseton
- Kloroaseton
Referensi[sunting | sunting sumber]
- ^ IUPAC (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. hlm. 739. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ a b c d e f William H. Sharkey (1979): "Polymerization through the carbon-sulfur double bond". Polymerization, series Advances in Polymer Science, volume 17, halaman 73–103. DOI:10.1007/3-540-07111-3_2
- ^ V.C.E. Burnop; K.G. Latham (1967). "Polythioacetone Polymer". Polymer. 8: 589–607. doi:10.1016/0032-3861(67)90069-9.
- ^ a b R.D. Lipscomb; W.H. Sharkey (1970). "Characterization and polymerization of thioacetone". Journal of Polymer Science Part A: Polymer Chemistry. 8 (8): 2187–2196. Bibcode:1970JPoSA...8.2187L. doi:10.1002/pol.1970.150080826.
- ^ Bailey, William J.; Chu, Hilda (1965). "Synthesis of polythioacetone". ACS Polymer Preprints. 6: 145–155.
- ^ Bohme, Horst; Pfeifer, Hans; Schneider, Erich (1942). "Dimeric thioketones". Berichte der Deutschen Chemischen Gesellschaft. 75B (7): 900–909. doi:10.1002/cber.19420750722. Catatan: Laporan awal ini salah mengira trimer sebagai monomer
- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamaV.C.E. Burnop, K.G 1967, Pages 589 - ^ Kroto, H.W.; Landsberg, B.M.; Suffolk, R.J.; Vodden, A. (1974). "The photoelectron and microwave spectra of the unstable species thioacetaldehyde, CH3CHS, and thioacetone, (CH3)2CS". Chemical Physics Letters. 29 (2): 265–269. Bibcode:1974CPL....29..265K. doi:10.1016/0009-2614(74)85029-3. ISSN 0009-2614.
- ^ a b Derek Lowe (11 Juni 2009). "Things I Won't Work With: Thioacetone". In The Pipeline.
- ^ E. Baumann; E. Fromm (1889). "Ueber Thioderivate der Ketone". Berichte der Deutschen Chemischen Gesellschaft. 22 (2): 2592–2599. doi:10.1002/cber.188902202151.
- ^ Chemical News and Journal of Industrial Science. Chemical news office. 1890. hlm. 219.
Pranala luar[sunting | sunting sumber]
- (Inggris) Tioaseton, NIST
- (Jerman) Tritioaseton, Aldrich