Proteasom
Proteasom adalah kompleks protein yang mendegradasi suatu protein yang tidak dibutuhkan atau rusak dengan cara proteolisis (reaksi kimia yang memutuskan ikatan peptida). Enzim yang membantu reaksi tersebut disebut protease.
Proteasom merupakan bagian dari mekanisme utama di dalam sel yang mengatur konsentrasi protein tertentu dan mendegradasi protein yang gagal melipat. Untuk bisa didegradasi, protein perlu ditandai dulu oleh protein kecil yang disebut ubiquitin, dengan bantuan katalisis enzim ubiquitin ligase. Setelah protein ditandai, hal ini memberi sinyal ke ligase lain untuk menempelkan molekul ubiquitin tambahan, membentuk rantai poliubiquitin. Selanjutnya, kompleks akan didegradasi oleh proteasom, menghasilkan peptida dengan panjang sekitar tujuh hingga delapan asam amino. Peptida-peptida dapat didegradasi lebih lanjut menjadi rangkaian asam amino yang lebih pendek dan digunakan dalam mensintesis protein baru.[1]
Proteasom ditemukan pada semua eukariota dan arkea, dan beberapa bakteri. Pada eukariota, proteasom terletak di dalam nukleus dan sitoplasma.[2]
Secara struktur, proteasom adalah kompleks silindris yang mengandung "inti" dari empat cincin bertumpuk yang membentuk pori pusat. Setiap cincin terdiri dari tujuh protein tunggal. Dua cincin bagian dalam terbuat dari tujuh subunit β yang mengandung tiga hingga tujuh situs aktif protease. Situs-situs ini terletak pada permukaan interior cincin, sehingga protein target harus masuk ke pori pusat sebelum terdegradasi. Dua cincin luar masing-masing berisi tujuh subunit α yang berfungsi untuk mempertahankan "gerbang" melalui protein-protein yang memasuki tabung. Subunit ini dikendalikan dengan mengikat struktur "tutup" atau partikel pengatur yang mengenali penanda (tag) poliubiquitin yang melekat pada substrat protein dan memulai proses degradasi. Sistem keseluruhan ubiquitinasi dan degradasi proteasomal dikenal sebagai sistem ubiquitin-proteasom (ubiquitin–proteasome system, UPS).[3]
Jalur degradasi proteasomal sangat penting untuk banyak proses seluler, termasuk siklus sel, regulasi ekspresi gen, dan respons terhadap stres oksidatif. Pentingnya degradasi proteolitik di dalam sel dan peran ubiquitin dalam jalur proteolitik diakui dalam Penghargaan Nobel Kimia 2004 kepada Aaron Ciechanover, Avram Hershko, dan Irwin Rose.[4]
Penemuan[sunting | sunting sumber]
Sebelum penemuan sistem ubiquitin-proteasom, degradasi protein dalam sel diperkirakan bergantung pada lisosom, suatu organel terikat membran dengan interior asam dan berisi protease yang dapat mendegradasi dan kemudian mendaur ulang protein eksogen dan organel tua atau rusak.[5] Namun, publikasi Joseph Etlinger dan Alfred L. Goldberg pada 1977 tentang degradasi protein yang bergantung pada ATP dalam retikulosit, yang tidak terdapat lisosom, menyarankan adanya mekanisme degradasi intraseluler kedua.[6] Pada 1978, ditunjukkan bahwa sistem terdiri dari beberapa rantai protein yang berbeda; ini merupakan hal baru pada saat itu.[7] Penelitian selanjutnya pada modifikasi histon mengarah pada identifikasi modifikasi kovalen yang tidak terduga dari protein histon oleh ikatan antara rantai samping lisin histon dan terminal C residu glisin dari ubiquitin, protein yang tidak diketahui fungsinya.[8] Kemudian ditemukan bahwa protein yang sebelumnya diidentifikasi terkait dengan degradasi proteolitik, yang dikenal sebagai ATP-dependent proteolysis factor 1 (APF-1), merupakan protein yang sama dengan ubiquitin.[9] Aktivitas proteolitik sistem ini diisolasi sebagai kompleks multi-protein yang awalnya disebut kompleks proteinase multikatalitik.[10] Kemudian, ditemukan kompleks proteolitik bergantung ATP yang bertanggung jawab untuk degradasi protein bergantung ubiquitin dan dinamakan proteasom 26S.[11]
Sebagian besar pekerjaan awal yang mengarah pada penemuan sistem proteasom ubiquitin terjadi pada akhir 1970-an dan awal 1980-an di laboratorium Avram Hershko (Technion, Institut Teknologi Israel), tempat Aaron Ciechanover menempuh studi pascasarjana. Penelitian Hershko selama setahun di laboratorium Irwin Rose, Pusat Kanker Fox Chase menghasilkan konsep penting; walau Rose kemudian menyatakan perannya kecil dalam penemuan tersebut. Ketiganya berbagi Hadiah Nobel Kimia 2004 untuk pekerjaan mereka dalam menemukan sistem UPS ini.[4]
Meskipun data mikroskop elektron mengungkapkan struktur cincin bertumpuk dari proteasom tersedia pada pertengahan 1980-an, struktur pertama dari partikel inti proteasom tidak didapatkan melalui kristalografi sinar-X sampai 1994.[12] Pada 2018, struktur atom pertama dari holoenzim proteasom 26S manusia dalam kompleks dengan substrat protein ter-poliubiquitilasi didapatkan melalui mikroskop elektron kriogenik (cryo-EM), mengungkapkan mekanisme tempat substrat dikenali, dideubiquitilasi, dibuka dan didegradasi oleh proteasom 26S manusia.[13]
Struktur dan organisasi[sunting | sunting sumber]
Subkomponen proteasom sering dinyatakan dengan koefisien sedimentasi Svedberg (dilambangkan S). Proteasom yang paling eksklusif digunakan pada mamalia adalah proteasom 26S sitosol: memiliki massa molekul sekitar 2000 kilodalton (kDa), mengandung satu subunit protein 20S dan dua subunit tutup pengatur 19S. Inti yang berongga menyediakan rongga tertutup untuk protein terdegradasi; bukaan di kedua ujung inti memungkinkan protein target masuk. Setiap ujung partikel inti berasosiasi dengan subunit pengatur 19S yang berisi beberapa situs aktif ATPase dan situs pengikatan ubiquitin; struktur inilah yang mengenali protein ter-poliubiquitinasi dan mentransfernya ke inti katalitik.[13] Bentuk alternatif dari subunit pengatur yang disebut partikel 11S dapat diasosiasikan dengan inti dasar dengan cara yang sama seperti partikel 19S; 11S mungkin memainkan peran dalam degradasi peptida asing seperti yang dihasilkan setelah infeksi oleh virus.[14]
Partikel inti 20S[sunting | sunting sumber]
Jumlah dan keragaman subunit yang terkandung dalam partikel inti 20S tergantung pada organisme. Jumlah subunit yang berbeda dan spesifik pada organisme multiseluler adalah lebih besar daripada uniseluler, dan lebih besar pada eukariota daripada pada prokariota. Semua partikel 20S terdiri dari empat struktur cincin heptamer bertumpuk yang terdiri dari dua jenis subunit yang berbeda; subunit α bersifat struktural, sedangkan subunit β sebagian besar bersifat katalitik. Subunit α merupakan pseudoenzim yang homolog dengan subunit β. Mereka dirakit dengan N-terminal berdekatan dengan subunit β.[15] Dua cincin terluar dalam tumpukan masing-masing terdiri dari tujuh subunit, yang berfungsi sebagai domain penambatan untuk partikel pengatur dan subunit alfa N-terminal (Pfam PF10584) membentuk gerbang yang menghalangi akses substrat yang tidak diatur ke rongga interior.[16] Dua cincin bagian dalam masing-masing terdiri dari tujuh subunit β dan di N-terminalnya mengandung situs aktif protease yang melakukan reaksi proteolisis.[17][18] Tiga aktivitas katalitik yang berbeda diidentifikasi dalam kompleks yang dimurnikan: hidrolisis seperti kimotripsin, seperti tripsin, dan peptidilglutamil-peptida.[12] Ukuran proteasom relatif dipertahankan dan sekitar 150 angstrom (Å) kali 115 Å. Ruang interior setidaknya pada lebar 53 Å, meski pintu masuknya bisa 13 Å, menunjukkan bahwa protein substrat harus setidaknya sebagian dibuka untuk masuk.[19]
Pada arkea seperti Thermoplasma acidophilum, semua subunit α dan subunit β adalah identik, sedangkan proteasom eukariotik seperti pada ragi mengandung tujuh jenis berbeda dari setiap subunit. Pada mamalia, subunit β1, β2, dan β5 bersifat katalitik; meskipun mereka memiliki mekanisme yang sama, mereka memiliki spesifisitas substrat yang berbeda, yakni serupa kimotripsin, serupa tripsin, dan peptidyl-glutamyl peptide-hydrolyzing (PHGH).[20] Bentuk alternatif yang dilambangkan β1i, β2i, dan β5i dapat diekspresikan dalam sel hematopoietik sebagai respons terhadap paparan sitokin proinflamasi, khususnya interferon gamma. Proteasom yang dirakit dengan subunit alternatif ini dikenal sebagai imunoproteasom,[21] yang spesifisitas substratnya diubah relatif terhadap proteasom normal.[22] Baru-baru ini proteasom alternatif diidentifikasi dalam sel manusia yang tidak memiliki subunit inti α3.[23] Proteasom ini dikenal sebagai proteasom α4-α4, membentuk partikel inti 20S yang mengandung subunit α4 tambahan sebagai pengganti subunit α3 yang hilang. Proteasom alternatif 'α4-α4' ini telah diketahui sebelumnya terdapat dalam ragi.[24] Meskipun fungsi pasti dari isoform proteasom ini masih belum diketahui, sel-sel yang mengekspresikan proteasom tersebut menunjukkan peningkatan resistensi terhadap toksisitas yang disebabkan oleh ion logam seperti kadmium.[23]
Partikel pengatur 19S[sunting | sunting sumber]
Partikel 19S pada eukariota terdiri dari 19 protein tunggal dan dapat dibagi menjadi dua sub-rakitan, basis 9-subunit yang mengikat langsung ke cincin dari partikel inti 20S, dan penutup 10-subunit. Enam dari sembilan protein pada basis merupakan subunit ATPase dari Famili AAA, dan homolog evolusioner dari ATPase ini ada di arkaea, yang disebut PAN (Proteasome-Activating Nucleotidase).[25] Asosiasi partikel 19S dan 20S membutuhkan pengikatan ATP ke subunit 19S ATPase, dan hidrolisis ATP diperlukan untuk kompleks yang dirakit untuk mendegradasi protein yang terlipat dan ter-ubiquitinasi. Langkah pembukaan substrat membutuhkan energi dari hidrolisis ATP, sedangkan pengikatan ATP dapat mendukung semua langkah lain yang diperlukan untuk degradasi protein, misalnya perakitan kompleks, pembukaan gerbang, translokasi, dan proteolisis.[26][27] Faktanya, pengikatan ATP ke ATPase dengan sendirinya mendukung degradasi cepat protein yang tidak dilipat. Namun, sementara hidrolisis ATP diperlukan untuk pembukaan saja, belum jelas apakah energi ini dapat digunakan dalam penggabungan beberapa langkah ini.[27]
Pada 2012, dua penelitian terpisah telah berhasil menjelaskan arsitektur molekul proteasom 26S dengan mikroskop elektron partikel tunggal.[28][29] Pada 2016, tiga penelitian terpisah telah menentukan struktur resolusi dekat-atomik pertama dari proteasom 26S manusia tanpa adanya substrat dengan cryo-EM.[30][31][32] Pada 2018, temuan besar berhasil menjelaskan mekanisme terperinci dari deubiquitilasi, inisiasi translokasi dan prosesi pembukaan substrat dengan menentukan tujuh struktur atom proteasom 26S yang melibatkan substrat secara bersamaan.[13] Pada pusat 19S, yang berbatasan langsung dengan 20S, terdapat AAA-ATPase (protein AAA) yang berkumpul menjadi cincin heteroheksamerik dengan urutan Rpt1/Rpt2/Rpt6/Rpt3/Rpt4/Rpt5. Cincin ini merupakan trimer dari dimer: Rpt1/Rpt2, Rpt6/Rpt3, dan Rpt4/Rpt5 yang berdimer melalui terminal N gulungan-melingkar. Gulungan melingkar ini menonjol dari cincin heksamerik. Partikel pengatur terbesar non-ATPase, Rpn1 dan Rpn2, mengikat ujung masing-masing Rpt1/2 dan Rpt6/3. Reseptor ubiquitin Rpn13 berikatan dengan Rpn2 dan melengkapi kompleks cub dasar. Bagian tutup menyelimuti setengah dari heksamer AAA-ATPase (Rpt6/Rpt3/Rpt4) dan langsung kontak dengan 20S melalui Rpn6, dan pada tingkat lebih rendah dengan Rpn5. Subunit Rpn9, Rpn5, Rpn6, Rpn7, Rpn3, dan Rpn12, yang secara struktural terkait satu sama lain dan dengan subunit dari kompleks COP9 dan eIF3 (karenanya disebut subunit PCI) berkumpul menjadi struktur seperti tapal kuda yang melingkupi heterodimer Rpn8/Rpn11. Rpn11, suatu enzim deubiquitinasi, ditempatkan di mulut heksamer AAA-ATPase, diposisikan secara ideal untuk menghilangkan bagian ubiquitin segera sebelum translokasi substrat ke dalam 20S. Reseptor ubiquitin kedua yang diidentifikasi hingga saat ini, Rpn10, diposisikan pada pinggiran tutup, dekat subunit Rpn8 dan Rpn9.
Perubahan konformasi dari 19S[sunting | sunting sumber]
Partikel pengatur 19S dalam holoenzim proteasom 26S telah diamati pada enam konformasi yang sangat berbeda tanpa adanya substrat hingga saat ini.[33][34] Ciri dari konfigurasi AAA-ATPase dalam keadaan energi rendah yang dominan ini yaitu susunan domain AAA seperti tangga atau lockwasher.[35][36] Dengan adanya ATP, tetapi tidak adanya substrat dari tiga alternatif konformasi, maka konformasi 19S yang kurang melimpah disetujui berbeda pada posisi tutup, sehubungan dengan modul AAA-ATPase.[37][34] Dengan keberadaan ATP-γS atau substrat, lebih banyak konformasi telah diamati yang menunjukkan perubahan struktural dramatis dari modul AAA-ATPase.[13][33][38][39] Beberapa konformasi terikat-substrat memiliki kemiripan yang tinggi dengan yang bebas-substrat, tetapi konformasi tidak sepenuhnya identik, khususnya dalam modul AAA-ATPase.[13][33] Sebelum perakitan 26S, partikel pengatur 19S dalam bentuk bebas juga telah diamati di tujuh konformasi.[40] Secara khusus, semua konformer ini agak berbeda dan menunjukkan fitur yang berbeda. Dengan demikian, partikel pengatur 19S dapat mengambil sampel setidaknya 20 konformasi pada kondisi fisiologis yang berbeda.
Regulasi 20S oleh 19S[sunting | sunting sumber]
Partikel pengatur 19S bertanggung jawab untuk memicu 20S untuk mendegradasi protein. Fungsi utama dari 19S regulator ATPase yaitu membuka gerbang di 20S yang menghalangi masuknya substrat ke dalam ruang degradasi.[41] Mekanisme bagaimana ATPase proteasomal membuka gerbang ini baru-baru ini telah diungkap.[42] Pembukaan gerbang 20S, dan dengan demikian degradasi substrat, membutuhkan C-terminal dari ATPase proteasomal, yang berisi motif tertentu (yaitu motif HbYX). ATPase C-terminal mengikat ke dalam kantong di bagian atas 20S, dan menambatkan kompleks ATPase ke kompleks proteolitik 20S, sehingga menggabungkan peralatan pembuka substrat dengan mesin degradasi 20S. Pengikatan C-terminal ke dalam kantong 20S ini dengan sendirinya merangsang pembukaan gerbang di 20S dengan cara yang sama seperti membuka pintu dengan kunci.[42] Mekanisme yang tepat di mana fungsi mekanisme "kunci-dalam-gembok" ini telah dijelaskan secara struktural dalam konteks proteasom 26S manusia pada resolusi mendekati atom, menunjukkan bahwa penyisipan lima C-terminal dari subunit ATPase Rpt1/2/ 3/5/6 ke dalam kantong permukaan 20S diperlukan untuk membuka gerbang 20S sepenuhnya.[43][13][44]
Partikel pengatur lainnya[sunting | sunting sumber]
Proteasom 20S juga dapat berasosiasi dengan tipe kedua dari partikel pengatur, partikel pengatur 11S, suatu struktur heptamerik yang tidak mengandung ATPase dan dapat mendorong degradasi peptida pendek tetapi tidak protein lengkap. Hal ini diduga karena kompleks tidak dapat membuka substrat yang lebih besar. Struktur ini juga dikenal sebagai PA28, REG, atau PA26.[45] Mekanisme yang mengikat partikel inti melalui ekor C-terminal dari subunitnya dan menginduksi perubahan konformasi cincin α untuk membuka gerbang 20S menunjukkan mekanisme serupa untuk partikel 19S.[46] Ekspresi partikel 11S diinduksi oleh interferon gamma dan berperan dalam hubungannya dengan subunit imunoproteasom, untuk pembentukan peptida yang mengikat kompleks histokompatibilitas utama.[47]
Jenis partikel pengatur non-ATPase lainnya adalah Blm10 (ragi) atau PA200/PSME4 (manusia). Partikel ini hanya membuka satu subunit α di gerbang 20S dan lalu terlipat menjadi kubah dengan pori yang sangat kecil di atasnya.[48]
Perakitan[sunting | sunting sumber]
Perakitan proteasom merupakan proses yang kompleks karena jumlah subunit yang harus bergabung untuk membentuk kompleks aktif. Subunit disintesis dengan "propeptida" N-terminal yang dimodifikasi pasca-translasi selama perakitan partikel 20S untuk memaparkan situs aktif proteolitik. Partikel 20S dirakit dari dua setengah proteasom, yang masing-masing terdiri dari cincin pro-β beranggota tujuh yang melekat pada cincin beranggota tujuh. Asosiasi cincin dari dua setengah proteasom memicu autolisis propeptida yang bergantung pada treonin untuk memaparkan situs aktif. Interaksi ini diperantarai terutama oleh jembatan garam dan interaksi hidrofobik antara alfa heliks yang terganggu oleh mutasi yang merusak kemampuan proteasom untuk berkumpul.[49] Perakitan setengah proteasom diinisiasi oleh perakitan subunit ke dalam cincin heptameriknya, membentuk cetakan untuk asosiasi cincin pro-β yang sesuai.
Baru-baru ini, proses perakitan partikel pengatur 19S telah dideskripsikan dengan baik. Partikel pengatur 19S berkumpul sebagai dua subkomponen yang berbeda, alas dan tutupnya. Perakitan kompleks dasar difasilitasi oleh empat pendamping perakitan, Hsm3/S5b, Nas2/p27, Rpn14/PAAF1, dan Nas6/gankirin (masing-masing nama pada ragi dan mamalia).[50] Pendamping perakitan ini mengikat subunit AAA-ATPase dan fungsi utamanya tampaknya untuk memastikan perakitan yang tepat dari cincin AAA-ATPase heteroheksamerik. Sampai saat ini masih dalam perdebatan apakah kompleks dasar dirakit secara terpisah, apakah perakitan dibuat oleh partikel inti 20S, atau apakah ada jalur perakitan alternatif. Selain empat pendamping perakitan, enzim deubiquitinasi Ubp6/Usp14 juga mempromosikan perakitan dasar, tetapi itu tidak esensial.[51] Penutup dirakit secara terpisah dalam urutan tertentu dan tidak memerlukan pendamping perakitan.[52]
Proses degradasi protein[sunting | sunting sumber]
Ubiquitinasi dan penargetan[sunting | sunting sumber]
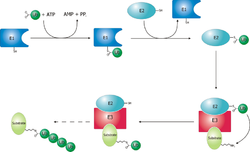
Protein ditargetkan untuk degradasi oleh proteasom dengan modifikasi kovalen dari residu lisin yang memerlukan reaksi terkoordinasi dari tiga enzim. Pada langkah pertama, enzim pengaktif ubiquitin (dikenal sebagai E1) menghidrolisis ATP dan adenilat molekul ubiquitin. Kemudian ditransfer ke residu sistein situs aktif E1 bersama dengan adenilasi ubiquitin kedua.[53] Ubiquitin ter-adenilasi ini kemudian ditransfer ke sistein enzim konjugasi ubiquitin (E2). Pada langkah terakhir, anggota kelas enzim yang sangat beragam yang dikenal sebagai ubiquitin ligase (E3) mengenali protein spesifik untuk di-ubiquitin dan mengkatalisis transfer ubiquitin dari E2 ke protein target. Protein target harus diberi label dengan setidaknya empat monomer ubiquitin (rantai poliubiquitin) sebelum dikenali oleh tutup proteasom.[54] Oleh karena itu, E3 yang memberikan kekhususan substrat pada sistem ini.[55] Jumlah protein E1, E2, dan E3 yang diekspresikan tergantung pada organisme dan jenis sel, tetapi ada banyak enzim E3 berbeda yang ada pada manusia, menunjukkan bahwa ada sejumlah besar target untuk sistem proteasom ubiquitin.
Mekanisme bagaimana protein ter-poliubiquitinasi ditargetkan ke proteasom tidak sepenuhnya dipahami. Beberapa cuplikan resolusi tinggi dari proteasom yang terikat pada protein ter-poliubiquitinasi menunjukkan bahwa reseptor ubiquitin mungkin dikoordinasikan dengan deubiquitinase Rpn11 untuk penargetan dan keterlibatan substrat awal.[13] Protein reseptor ubiquitin memiliki domain N-terminal ubiquitin-like (UBL) dan satu atau lebih domain ubiquitin-associated (UBA). Domain UBL dikenali oleh tutup proteasom 19S dan domain UBA mengikat ubiquitin melalui bundel tiga heliks. Protein reseptor ini dapat mengawal protein ter-poliubiquitinasi ke proteasom, meskipun interaksi ini dan regulasinya secara spesifik masih belum jelas.[56]
Protein ubiquitin itu sendiri memiliki panjang 76 asam amino dan dinamai demikian karena sifatnya yang ada di mana-mana, karena memiliki urutan yang sangat lestari dan ditemukan di semua organisme eukariotik yang dikenal.[57] Gen yang menyandi ubiquitin pada eukariota diatur dalam pengulangan tandem, bisa dikarenakan tuntutan transkripsi yang berat pada gen ini untuk menghasilkan ubiquitin yang cukup untuk sel.[58] Telah diusulkan bahwa ubiquitin merupakan protein yang paling lambat berevolusi yang diketahui hingga saat ini. Ubiquitin mengandung tujuh residu lisin dimana ubiquitin lain dapat diikat, menghasilkan berbagai jenis rantai poliubiquitin.[59][60] Rantai tempat setiap ubiquitin tambahan terkait dengan lisin 48 dari ubiquitin sebelumnya memiliki peran dalam penargetan proteasom, sementara jenis rantai lain mungkin terlibat dalam proses lain.[61][62]
Pembukaan dan translokasi[sunting | sunting sumber]
Setelah protein diubikitinasi, protein tersebut dikenali oleh partikel pengatur 19S dalam langkah pengikatan yang bergantung pada ATP.[13][63] Protein substrat kemudian harus memasuki bagian dalam partikel 20S untuk bersentuhan dengan situs aktif proteolitik. Karena kanal pusat partikel 20S sempit dan dibatasi oleh ekor N-terminal dari subunit cincin, substrat setidaknya harus dibuka sebagian sebelum memasuki inti.[13] Bagian dari substrat yang tidak dilipat ke dalam inti disebut translokasi dan harus terjadi setelah de-ubiquitinasi.[13][63] Namun, urutan substrat di-deubiquitinasi dan dibuka belum jelas.[64][65] Proses mana yang merupakan tahap pembatas laju dalam reaksi proteolisis keseluruhan bergantung pada substrat spesifik; untuk beberapa protein, proses pembukaannya membatasi kecepatan, sementara deubiquitinasi merupakan langkah paling lambat untuk protein lain.[66] Sejauh mana substrat harus dibuka sebelum translokasi disarankan menjadi sekitar 20 residu asam amino oleh struktur atom proteasom 26S yang terikat substrat dalam keadaan kompatibel deubiquitilasi,[13] tetapi struktur tersier bersifat penting, dan khususnya interaksi nonlokal seperti ikatan disulfida, cukup untuk menghambat degradasi.[67] Kehadiran segmen protein yang tidak teratur secara intrinsik dengan ukuran yang cukup, baik pada terminal protein atau secara internal, juga telah diusulkan untuk memfasilitasi inisiasi degradasi yang efisien.[68][69]
Gerbang yang dibentuk oleh subunit mencegah peptida yang lebih panjang dari sekitar empat residu memasuki bagian dalam partikel 20S. Molekul ATP yang terikat sebelum langkah pengenalan awal dihidrolisis sebelum translokasi. Sementara energi dibutuhkan untuk membuka substrat, itu tidak diperlukan untuk translokasi.[70][71] Proteasom 26S yang dirakit dapat mendegradasi protein yang tidak dilipat dengan adanya analog ATP yang tidak dapat dihidrolisis, tetapi tidak dapat menurunkan protein yang terlipat, menunjukkan bahwa energi dari hidrolisis ATP digunakan untuk membuka substrat.[70] Lewatnya substrat yang tidak dilipat melalui gerbang yang terbuka terjadi melalui difusi terfasilitasi jika tutup 19S dalam keadaan terikat ATP.[70]
Mekanisme untuk pembukaan protein globular bersifat umum, tetapi agak tergantung pada urutan asam amino. Urutan panjang glisin dan alanin bergantian telah terbukti menghambat pembukaan substrat, menurunkan efisiensi degradasi proteasomal; hal ini menghasilkan pelepasan produk sampingan yang terdegradasi sebagian, mungkin karena pemisahan hidrolisis ATP dan langkah-langkah pembukaan.[72] Pengulangan glisin-alanin seperti itu juga ditemukan di alam, misalnya dalam fibroin sutra; khususnya, produk gen virus Epstein-Barr tertentu yang mengandung urutan ini dapat menghentikan proteasom, membantu virus menyebar dengan mencegah presentasi antigen pada kompleks histokompatibilitas utama.[73]
Proteolisis[sunting | sunting sumber]
Proteasom berfungsi sebagai endoprotease.[74][75][76][77] Mekanisme proteolisis oleh subunit β dari partikel inti 20S adalah melalui serangan nukleofilik yang bergantung pada treonin. Mekanisme ini mungkin bergantung pada molekul air untuk deprotonasi hidroksil treonin reaktif. Degradasi terjadi di dalam ruang tengah yang dibentuk oleh asosiasi dua cincin dan biasanya tidak melepaskan produk yang terdegradasi sebagian, sebaliknya mereduksi substrat menjadi polipeptida pendek yang biasanya memiliki panjang 7-9 residu, meskipun dapat berkisar dari 4 hingga 25 residu, tergantung pada organisme dan substrat. Mekanisme biokimia yang menentukan panjang produk tidak sepenuhnya diketahui.[78] Meskipun ketiga subunit katalitik memiliki mekanisme yang sama, subunit-subunit memiliki spesifisitas substrat yang sedikit berbeda, yakni substrat serupa kimotripsin, serupa tripsin, dan peptidyl-glutamyl peptide-hydrolyzing (PHGH). Variasi dalam spesifisitas ini merupakan hasil dari kontak interatomik dengan residu lokal di dekat situs aktif setiap subunit. Setiap subunit katalitik juga memiliki residu lisin yang diperlukan untuk proteolisis.[79]
Meskipun proteasom biasanya menghasilkan fragmen peptida yang sangat pendek, dalam beberapa kasus produk ini merupakan molekul yang aktif secara biologis dan fungsional. Faktor transkripsi tertentu yang mengatur ekspresi gen spesifik, termasuk satu komponen kompleks mamalia NF-κB, disintesis sebagai prekursor tidak aktif yang ubiquitinasi dan degradasi proteasomal selanjutnya mengubahnya menjadi bentuk aktif. Aktivitas tersebut membutuhkan proteasom untuk membelah protein substrat secara internal, daripada secara proses menurunkannya dari satu terminal. Telah disarankan bahwa loop panjang pada permukaan protein ini berfungsi sebagai substrat proteasomal dan memasuki rongga pusat, sementara sebagian besar protein tetap berada di luar. Efek serupa telah diamati pada protein ragi; mekanisme degradasi selektif ini dikenal sebagai regulated ubiquitin/proteasome dependent processing (RUP).[80]
Degradasi tidak tergantung ubiquitin[sunting | sunting sumber]
Meskipun sebagian besar substrat proteasomal harus ada ubiquitinasi sebelum didegradasi, terdapat beberapa pengecualian untuk aturan umum ini, terutama ketika proteasom memainkan peran normal dalam pengolahan protein pasca-translasi. Contohnya, aktivasi proteasomal NF-kB dengan memproses p105 menjadi p50 melalui proteolisis internal.[81] Beberapa protein yang dihipotesiskan menjadi tidak stabil karena daerah yang tidak terstruktur secara intrinsik,[82] terdegradasi secara tidak bergantung ubiquitin. Contoh paling terkenal dari substrat proteasom yang tidak bergantung pada ubiquitin yaitu enzim ornitin dekarboksilase.[83] Mekanisme tidak bergantung ubiquitin yang menargetkan regulator siklus sel utama seperti p53 juga telah dilaporkan, meskipun p53 juga sasaran pada degradasi yang bergantung pada ubiquitin.[84] Akhirnya, protein yang secara struktural abnormal, salah lipatan, atau sangat teroksidasi juga sasaran pada degradasi tidak bergantung ubiquitin dan tidak bergantung 19S dalam kondisi stres seluler.[85]
Evolusi[sunting | sunting sumber]

Proteasom 20S ada di mana-mana dan penting dalam eukariota dan arkaea. Ordo bakteri Actinomycetales, juga berbagi homolog dari proteasom 20S, sedangkan sebagian besar bakteri memiliki gen kejutan panas hslV dan hslU, yang produk gennya adalah protease multimerik yang tersusun dalam cincin dua lapis dan ATPase.[86] Protein hslV telah dihipotesiskan menyerupai nenek moyang proteasom 20S.[87][88] Secara umum, HslV tidak esensial pada bakteri, sedangkan beberapa protista memiliki sistem 20S dan hslV.[86] Banyak bakteri juga memiliki homolog lain dari proteasom dan ATPase terkait, terutama ClpP dan ClpX. Redundansi ini menjelaskan mengapa sistem HslUV tidak esensial.
Analisis urutan menunjukkan bahwa subunit katalitik menyimpang lebih awal dalam evolusi daripada subunit yang dominan struktural. Pada bakteri yang mengekspresikan proteasom 20S, subunit memiliki identitas urutan yang tinggi terhadap subunit arkea dan eukariotik, sedangkan identitas urutan jauh lebih rendah. Adanya proteasom 20S pada bakteri dapat berasal dari transfer gen horizontal, sedangkan diversifikasi subunit di antara eukariota dianggap berasal dari beberapa peristiwa duplikasi gen.[86]
Peran pada proses seluler[sunting | sunting sumber]
Kontrol siklus sel[sunting | sunting sumber]
Progresi siklus sel dikendalikan oleh aksi berurutan dari cyclin-dependent kinase (CDK), diaktifkan oleh siklin spesifik yang membatasi fase-fase siklus sel. Siklin mitosis, yang bertahan di dalam sel hanya beberapa menit, memiliki salah satu rentang hidup terpendek dari semua protein intraseluler. Setelah kompleks CDK-siklin menjalankan fungsinya, siklin tersebut dipoliubiquitinasi dan dihancurkan oleh proteasom, yang memberikan arah untuk siklus sel. Secara khusus, sel keluar dari fase mitosis membutuhkan disosiasi yang tergatung proteasom yaitu komponen regulator siklin B dari maturation-promoting factor (MPF).[89] Pada sel vertebrata, sel dapat keluar dari fase mitosis tanpa pemisahan kromosom yang tepat (mitotic slippage), meskipun spindle assembly checkpoint (SAC) telah menundanya.[90]
Pos pemeriksaan siklus sel sebelumnya seperti pemeriksaan titik pasca-pembatasan antara fase G1 dan fase S juga melibatkan degradasi proteasomal dari siklin A, yang ubiquitinasinya dipromosikan oleh kompleks pemacu anafase (APC), sebuah ligase ubiquitin E3.[91] APC dan kompleks protein Skp1/Cul1/F-box (kompleks SCF) merupakan dua pengatur utama degradasi siklin dan kontrol pos pemeriksaan; SCF sendiri diatur oleh APC melalui ubiquitinasi protein adaptor, Skp2, yang mencegah aktivitas SCF sebelum transisi G1-S.[92]
Komponen individu dari partikel 19S memiliki peran pengaturannya sendiri. Gankirin, suatu onkoprotein yang baru-baru ini diidentifikasi, merupakan salah satu subkomponen 19S yang juga mengikat erat CDK4 kinase yang bergantung pada siklin dan memainkan peran kunci dalam mengenali p53, melalui afinitasnya terhadap ubiquitin ligase MDM2. Gankirin bersifat anti-apoptosis dan telah terbukti diekspresikan secara berlebihan pada beberapa jenis sel tumor seperti karsinoma hepatoseluler.[93]
Seperti eukariota, beberapa arkea juga menggunakan proteasom untuk mengontrol siklus sel, khususnya dengan mengontrol pembelahan sel yang diperantarai ESCRT-III.[94]
Pengaturan pertumbuhan tanaman[sunting | sunting sumber]
Pada tumbuhan, pensinyalan oleh auksin atau fitohormon yang mengatur arah dan tropisme pertumbuhan tanaman, akan menginduksi penargetan kelas penekan faktor transkripsi yang dikenal sebagai protein Aux/IAA untuk degradasi proteasomal. Protein ini diubikitinasi oleh SCFTIR1, atau SCF dalam kompleks dengan reseptor auksin TIR1. Degradasi protein Aux/IAA berikutnya menekan faktor transkripsi dalam keluarga faktor respons auksin (auxin-response factor, ARF) dan menginduksi ekspresi gen yang diregulasi oleh ARF.[95] Konsekuensi seluler dari aktivasi ARF tergantung pada jenis tanaman dan tahap perkembangan, tetapi terlibat dalam mengarahkan pertumbuhan akar dan urat daun. Respons spesifik terhadap derepresi ARF diperkirakan diperantarai oleh spesifisitas dalam penyatuan protein ARF dan Aux/IAA individu.[96]
Apoptosis[sunting | sunting sumber]
Baik sinyal internal maupun eksternal dapat menyebabkan induksi apoptosis atau kematian sel terprogram. Dekonstruksi komponen seluler yang dihasilkan terutama dilakukan oleh protease khusus yang dikenal sebagai caspase, tetapi proteasom juga memainkan peran penting dan beragam dalam proses apoptosis. Keterlibatan proteasom dalam proses ini ditunjukkan oleh peningkatan ubiquitinasi protein, dan enzim E1, E2, dan E3 yang diamati jauh sebelum apoptosis.[97][98][99] Selama apoptosis, proteasom yang terlokalisasi pada nukleus juga telah diamati bertranslokasi ke lekukan membran luar yang merupakan karakteristik dari apoptosis.[100]
Penghambatan proteasom memiliki efek yang berbeda pada induksi apoptosis pada jenis sel yang berbeda. Secara umum, proteasom tidak diperlukan untuk apoptosis, meskipun menghambatnya pro-apoptosis pada sebagian besar jenis sel yang telah dipelajari. Apoptosis diperantarai melalui gangguan degradasi diatur protein siklus sel pro-pertumbuhan. Namun, beberapa sel, khususnya kultur primer sel fase G0 dan sel berdiferensiasi seperti timosit dan neuron, dicegah dari menjalani apoptosis pada paparan inhibitor proteasom. Mekanisme untuk efek ini tidak jelas, tetapi dihipotesiskan spesifik untuk sel dalam keadaan fase G0, atau sebagai hasil dari aktivitas diferensial JNK pro-apoptosis kinase.[101] Kemampuan inhibitor proteasom untuk menginduksi apoptosis pada sel yang membelah dengan cepat telah dimanfaatkan dalam beberapa agen kemoterapi yang dikembangkan baru-baru ini seperti bortezomib dan salinosporamide A.
Respons pada stres seluler[sunting | sunting sumber]
Sebagai respons terhadap tekanan seluler – seperti infeksi, sengatan panas, atau kerusakan oksidatif –diekspresikan protein kejutan panas yang mengidentifikasi protein yang salah lipatan atau tidak dilipat dan menargetkannya untuk degradasi proteasomal. Baik Hsp27 dan Hsp90 — protein pendamping telah terlibat dalam meningkatkan aktivitas sistem ubiquitin-proteasom, meskipun mereka bukan peserta langsung dalam proses tersebut.[102] Hsp70, di sisi lain, mengikat tambalan hidrofobik yang terbuka pada permukaan protein yang salah lipatan dan merekrut ligase ubiquitin E3 seperti CHIP untuk menandai protein untuk degradasi proteasomal.[103] Protein CHIP (carboxyl terminus dari protein yang berinteraksi dengan Hsp70) sendiri diatur melalui penghambatan interaksi antara enzim E3 CHIP dan mitra pengikatan E2-nya.[104]
Mekanisme serupa ada untuk mempromosikan degradasi protein yang rusak secara oksidatif melalui sistem proteasom. Secara khusus, proteasom yang terlokalisasi pada nukleus diatur oleh PARP dan secara aktif menurunkan histon yang teroksidasi secara tidak tepat.[105] Protein teroksidasi, yang sering membentuk agregat amorf besar di dalam sel, dapat didegradasi langsung oleh partikel inti 20S tanpa tutup pengatur 19S dan tidak memerlukan hidrolisis ATP atau penandaan dengan ubiquitin.[106] Namun, tingkat kerusakan oksidatif yang tinggi meningkatkan tingkat ikatan silang antara fragmen protein, membuat agregat tahan terhadap proteolisis. Jumlah dan ukuran yang lebih besar dari agregat yang sangat teroksidasi tersebut berhubungan dengan penuaan.[107]
Disregulasi sistem proteasom ubiquitin dapat berkontribusi pada beberapa penyakit saraf. Hal ini dapat menyebabkan tumor otak seperti astrositoma.[108] Pada beberapa penyakit neurodegeneratif awitan lambat yang berbagi agregasi protein yang gagal melipat sebagai fitur umum, seperti penyakit Parkinson dan penyakit Alzheimer, agregat besar protein yang gagal melipat dapat terbentuk dan kemudian mengakibatkan neurotoksisitas, melalui mekanisme yang belum dipahami dengan baik. Penurunan aktivitas proteasom telah disarankan sebagai penyebab agregasi dan pembentukan badan Lewy pada Parkinson.[109] Hipotesis ini didukung oleh pengamatan bahwa model ragi Parkinson lebih rentan terhadap toksisitas dari α-sinuklein, komponen protein utama badan Lewy, dalam kondisi aktivitas proteasom rendah.[110] Gangguan aktivitas proteasomal dapat mendasari gangguan kognitif seperti gangguan spektrum autisme, dan penyakit otot dan saraf seperti miopati tubuh inklusi.[108]
Peran pada sistem imun[sunting | sunting sumber]
Proteasom memainkan peran langsung tetapi penting dalam fungsi sistem imun adaptif.[111] Antigen peptida disajikan oleh protein kompleks histokompatibilitas utama (MHC) kelas I pada permukaan sel penyaji antigen. Peptida ini adalah produk degradasi protein proteasomal yang berasal dari patogen. Meskipun proteasom yang diekspresikan secara konstitutif dapat berpartisipasi dalam proses ini, kompleks khusus yang terdiri dari protein, yang ekspresinya diinduksi oleh interferon gamma, merupakan produsen utama peptida yang optimal dalam ukuran dan komposisi untuk pengikatan MHC. Protein ini yang ekspresinya meningkat selama respons imun termasuk partikel pengatur 11S, yang peran biologis utamanya yaitu mengatur produksi ligan MHC, dan subunit khusus yang disebut β1i, β2i, dan β5i dengan spesifisitas substrat yang berubah. Kompleks yang dibentuk dengan subunit β khusus dikenal sebagai imunoproteasom.[112] Subunit varian β5i lainnya, β5t, diekspresikan dalam timus, yang mengarah ke "timoproteasom" spesifik-timus yang fungsinya masih belum jelas.[113]
Kekuatan ikatan ligan MHC kelas I tergantung pada komposisi ligan C-terminal, karena peptida terikat oleh ikatan hidrogen dan dengan kontak dekat dengan daerah yang disebut "kantong B" pada permukaan MHC. Banyak alel MHC kelas I lebih menyukai residu C-terminal hidrofobik, dan kompleks imunoproteasom lebih cenderung menghasilkan C-terminal hidrofobik.[114]
Karena perannya dalam menghasilkan bentuk aktif NF-kB, pengatur ekspresi sitokin anti-apoptosis dan proinflamasi, aktivitas proteasomal telah dikaitkan dengan penyakit inflamasi dan autoimun. Peningkatan tingkat aktivitas proteasom berkorelasi dengan aktivitas penyakit dan telah terlibat dalam penyakit autoimun termasuk lupus eritematosus sistemik dan artritis reumatoid.[115]
Proteasom juga terlibat dalam proteolisis yang dimediasi antibodi intraseluler dari virion yang terikat antibodi. Dalam jalur netralisasi ini, TRIM21 (protein dari keluarga motif tripartit) berikatan dengan imunoglobulin G untuk mengarahkan virion ke proteasom di mana protein ini terdegradasi.[116]
Peran pada penyakit[sunting | sunting sumber]
Proteasom dan subunitnya memiliki signifikansi klinis karena adanya gangguan perakitan kompleks atau proteasom disfungsional dapat dikaitkan dengan patofisiologi yang mendasari penyakit tertentu, dan proteasom dapat dimanfaatkan sebagai target obat untuk terapi. Baru-baru ini, juga banyak upaya telah dilakukan untuk mempertimbangkan proteasom untuk pengembangan penanda dan strategi diagnostik baru.
Proteasom membentuk komponen penting untuk sistem ubiquitin-proteasom (UPS)[117] dan kontrol kualitas protein seluler yang sesuai. Ubiquitinasi protein dan proteolisis dan degradasi selanjutnya oleh proteasom merupakan mekanisme penting dalam regulasi siklus sel, pertumbuhan dan diferensiasi sel, transkripsi gen, transduksi sinyal dan apoptosis.[118] Selanjutnya, perakitan dan fungsi kompleks proteasom yang dikompromikan menyebabkan berkurangnya aktivitas proteolitik dan akumulasi spesies protein yang rusak atau salah lipat. Akumulasi protein tersebut dapat berkontribusi pada patogenesis dan karakteristik fenotipik pada penyakit neurodegeneratif,[119][120] penyakit kardiovaskular,[121][122] respons inflamasi dan penyakit autoimun,[123][124] dan respons kerusakan DNA sistemik yang mengarah pada keganasan.[125]
Beberapa penelitian eksperimental dan klinis telah menunjukkan bahwa penyimpangan dan deregulasi UPS berkontribusi pada patogenesis beberapa gangguan neurodegeneratif dan myodegeneratif, termasuk penyakit Alzheimer,[126] penyakit Parkinson,[127] dan penyakit Pick,[128][129] sklerosis lateral amiotrofik (ALS),[128] penyakit Huntington,[73] penyakit Creutzfeldt-Jakob,[130] dan penyakit neuron motorik, penyakit poliglutamin (PolyQ), distrofi otot,[131] dan beberapa bentuk penyakit neurodegeneratif yang jarang terkait dengan demensia.[128]
Sebagai bagian dari sistem ubiquitin-proteasom (UPS), proteasom mempertahankan homeostasis protein jantung dan dengan demikian memainkan peran penting dalam cedera iskemik jantung,[132] hipertrofi ventrikel,[133] dan gagal jantung.[134]
Selain itu, bukti terakumulasi bahwa UPS memainkan peran penting dalam transformasi keganasan. Proteolisis UPS memainkan peran utama dalam respons sel kanker terhadap sinyal stimulasi yang sangat penting untuk perkembangan kanker. Oleh karena itu, ekspresi gen melalui degradasi faktor transkripsi, seperti p53, c-jun, c-Fos, NF-κB, c-Myc, HIF-1α, MATα2, STAT3, protein pengikat elemen yang diatur sterol dan reseptor androgen semuanya dikendalikan oleh UPS dan dengan demikian terlibat dalam perkembangan berbagai keganasan.[135][136] Selain itu, UPS mengatur degradasi produk gen supresor tumor seperti adenomatous polyposis coli (APC) pada kanker kolorektal, retinoblastoma (Rb), dan penekan tumor von Hippel–Lindau (VHL), serta sejumlah proto-onkogen (Raf, Myc, Myb, Rel, Src, Mos, ABL). UPS juga terlibat dalam regulasi respon inflamasi. Aktivitas ini biasanya dikaitkan dengan peran proteasom dalam aktivasi NF-κB yang selanjutnya mengatur ekspresi sitokin pro-inflamasi seperti TNF-α, IL-β, IL-8, molekul adhesi (ICAM-1, VCAM-1, P-selektin), prostaglandin, dan nitrogen monoksida (NO).[123] Selain itu, UPS juga berperan dalam respons inflamasi sebagai pengatur proliferasi leukosit, terutama melalui proteolisis siklin dan degradasi inhibitor CDK.[137] Terakhir, pasien penyakit autoimun dengan SLE, sindrom Sjögren dan rheumatoid arthritis (RA) secara dominan menunjukkan proteasom yang bersirkulasi yang dapat diterapkan sebagai biomarker klinis.[138]
Inhibitor proteasom[sunting | sunting sumber]
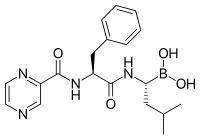
Inhibitor proteasom memiliki aktivitas anti-tumor yang efektif dalam kultur sel yaitu menginduksi apoptosis dengan mengganggu degradasi yang diatur dari protein siklus sel pro-pertumbuhan. Pendekatan selektif menginduksi apoptosis dalam sel tumor telah terbukti efektif dalam model hewan dan percobaan manusia.
Laktasistin, suatu produk alami yang disintesis oleh bakteri Streptomyces, merupakan inhibitor proteasom non-peptida pertama yang ditemukan,[139] dan digunakan secara luas sebagai bahan penelitian dalam biokimia dan biologi sel. Laktasistin secara kovalen memodifikasi treonin terminal amino dari subunit katalitik dari proteasom, khususnya subunit β5 yang bertanggung jawab atas aktivitas proteasom serupa kimotripsin. Penemuan ini membantu menetapkan proteasom sebagai kelas protease baru yang mekanistik: protease treonin terminal amino.
Bortezomib (Boronated MG132), sebuah molekul yang dipasarkan sebagai Velcade, adalah inhibitor proteasom pertama yang dalam penggunaan klinis sebagai agen kemoterapi.[140][141] Bortezomib digunakan dalam pengobatan multiple myeloma.[142] Khususnya, multiple myeloma telah diamati menghasilkan peningkatan kadar peptida turunan proteasom dalam serum darah yang menurun ke tingkat normal sebagai respons terhadap kemoterapi yang berhasil.[143] Penelitian pada hewan telah menunjukkan bahwa bortezomib dapat juga memiliki efek klinis yang signifikan pada kanker pankreas.[144] Penelitian pra-klinis dan klinis awal telah dimulai untuk menguji efektivitas bortezomib dalam mengobati kanker terkait sel B lainnya,[145] khususnya beberapa jenis limfoma non-Hodgkin.[146][147] Hasil klinis juga tampaknya membenarkan penggunaan inhibitor proteasom yang dikombinasikan dengan kemoterapi, untuk leukemia limfoblastik akut sel B.[148] Inhibitor proteasom dapat membunuh beberapa jenis sel leukemia yang resisten terhadap glukokortikoid.[149]
Ritonavir dikembangkan sebagai inhibitor protease dan digunakan untuk menargetkan infeksi HIV. Namun, telah terbukti menghambat proteasom serta protease bebas; secara spesifik, aktivitas proteasom serupa kimotripsin dihambat oleh ritonavir, sedangkan aktivitas serupa tripsin agak meningkat.[150] Studi pada model hewan menunjukkan bahwa ritonavir mungkin memiliki efek penghambatan pada pertumbuhan sel glioma.[151]
Inhibitor proteasom juga menjanjikan dalam mengobati penyakit autoimun pada model hewan. Misalnya, penelitian pada tikus yang membawa cangkok kulit manusia menemukan pengurangan ukuran lesi dari psoriasis setelah pengobatan dengan inhibitor proteasom.[152] Inhibitor juga menunjukkan efek positif pada model asma tikus.[153] Bahan-bahan dari alam saat ini juga dilirik karena potensi aksinya sebagai inhibitor proteasom.[154]
Pelabelan dan inhibitor proteasom juga menarik dalam laboratorium untuk studi aktivitas proteasomal dalam sel in vitro dan in vivo. Inhibitor proteasom yang paling umum digunakan yaitu laktasistin dan peptida aldehid MG132 yang awalnya dikembangkan oleh laboratorium Goldberg. Inhibitor fluoresen juga telah dikembangkan untuk secara khusus memberi label pada situs aktif dari proteasom yang dirakit.[155]
Referensi[sunting | sunting sumber]
- ^ Bard, Jared A.M.; Goodall, Ellen A.; Greene, Eric R.; Jonsson, Erik; Dong, Ken C.; Martin, Andreas (2018-06-20). "Structure and Function of the 26S Proteasome". Annual Review of Biochemistry (dalam bahasa Inggris). 87 (1): 697–724. doi:10.1146/annurev-biochem-062917-011931. ISSN 0066-4154. PMC 6422034
 . PMID 29652515. Diarsipkan dari versi asli tanggal 2020-11-15. Diakses tanggal 2022-02-22.
. PMID 29652515. Diarsipkan dari versi asli tanggal 2020-11-15. Diakses tanggal 2022-02-22.
- ^ Peters, J. M.; Franke, W. W.; Kleinschmidt, J. A. (1994-03-11). "Distinct 19 S and 20 S subcomplexes of the 26 S proteasome and their distribution in the nucleus and the cytoplasm". The Journal of Biological Chemistry. 269 (10): 7709–7718. ISSN 0021-9258. PMID 8125997.
- ^ Nassif, Nicholas D.; Cambray, Samantha E.; Kraut, Daniel A. (2014-05). "Slipping up: partial substrate degradation by ATP-dependent proteases". IUBMB life. 66 (5): 309–317. doi:10.1002/iub.1271. ISSN 1521-6551. PMID 24823973.
- ^ a b "The Nobel Prize in Chemistry 2004". NobelPrize.org (dalam bahasa Inggris). Diakses tanggal 2022-02-18.
- ^ Lodish H, Berk A, Matsudaira P, Kaiser CA, Krieger M, Scott MP, Zipursky SL, Darnell J (2004). "3". Molecular cell biology (edisi ke-5th). New York: W.H. Freeman and CO. hlm. 66–72. ISBN 978-0-7167-4366-8.
- ^ Etlinger JD, Goldberg AL (January 1977). "A soluble ATP-dependent proteolytic system responsible for the degradation of abnormal proteins in reticulocytes". Proceedings of the National Academy of Sciences of the United States of America. 74 (1): 54–8. Bibcode:1977PNAS...74...54E. doi:10.1073/pnas.74.1.54. PMC 393195
 . PMID 264694.
. PMID 264694.
- ^ Ciechanover, A.; Heller, H.; Katz-Etzion, R.; Hershko, A. (1981-02-01). "Activation of the heat-stable polypeptide of the ATP-dependent proteolytic system". Proceedings of the National Academy of Sciences (dalam bahasa Inggris). 78 (2): 761–765. doi:10.1073/pnas.78.2.761. ISSN 0027-8424. PMC 319882
 . PMID 6262770.
. PMID 6262770.
- ^ Goldknopf IL, Busch H (March 1977). "Isopeptide linkage between nonhistone and histone 2A polypeptides of chromosomal conjugate-protein A24". Proceedings of the National Academy of Sciences of the United States of America. 74 (3): 864–8. Bibcode:1977PNAS...74..864G. doi:10.1073/pnas.74.3.864. PMC 430507
 . PMID 265581.
. PMID 265581.
- ^ Ciechanover A (September 2005). "Early work on the ubiquitin proteasome system, an interview with Aaron Ciechanover. Interview by CDD". Cell Death and Differentiation. 12 (9): 1167–77. doi:10.1038/sj.cdd.4401691. PMID 16094393.
- ^ Djaballah, H; Rowe, A J; Harding, S E; Rivett, A J (1993-06-15). "The multicatalytic proteinase complex (proteasome): structure and conformational changes associated with changes in proteolytic activity". Biochemical Journal (dalam bahasa Inggris). 292 (3): 857–862. doi:10.1042/bj2920857. ISSN 0264-6021. PMC 1134193
 . PMID 8318014.
. PMID 8318014.
- ^ Hough R, Pratt G, Rechsteiner M (June 1987). "Purification of two high molecular weight proteases from rabbit reticulocyte lysate". The Journal of Biological Chemistry. 262 (17): 8303–13. doi:10.1016/S0021-9258(18)47564-3. PMID 3298229.
- ^ a b Tanaka, Keiji (2009). "The proteasome: overview of structure and functions". Proceedings of the Japan Academy. Series B, Physical and Biological Sciences. 85 (1): 12–36. doi:10.2183/pjab.85.12. ISSN 1349-2896. PMC 3524306
 . PMID 19145068.
. PMID 19145068.
- ^ a b c d e f g h i j k Dong Y, Zhang S, Wu Z, Li X, Wang WL, Zhu Y, Stoilova-McPhie S, Lu Y, Finley D, Mao Y (November 2018). "Cryo-EM structures and dynamics of substrate-engaged human 26S proteasome". Nature. 565 (7737): 49–55. doi:10.1038/s41586-018-0736-4. PMC 6370054
 . PMID 30479383.
. PMID 30479383.
- ^ Wang J, Maldonado MA (August 2006). "The ubiquitin-proteasome system and its role in inflammatory and autoimmune diseases". Cellular & Molecular Immunology. 3 (4): 255–61. PMID 16978533.
- ^ Stadtmueller, BM; Hill, CP (7 January 2011). "Proteasome activators". Molecular Cell. 41 (1): 8–19. doi:10.1016/j.molcel.2010.12.020. PMC 3040445
 . PMID 21211719.
. PMID 21211719.
- ^ Smith DM, Chang SC, Park S, Finley D, Cheng Y, Goldberg AL (September 2007). "Docking of the proteasomal ATPases' carboxyl termini in the 20S proteasome's alpha ring opens the gate for substrate entry". Molecular Cell. 27 (5): 731–44. doi:10.1016/j.molcel.2007.06.033. PMC 2083707
 . PMID 17803938.
. PMID 17803938.
- ^ Kumar Deshmukh, Fanindra; Yaffe, Dana; Olshina, Maya; Ben-Nissan, Gili; Sharon, Michal (2019-05-16). "The Contribution of the 20S Proteasome to Proteostasis". Biomolecules (dalam bahasa Inggris). 9 (5): 190. doi:10.3390/biom9050190. ISSN 2218-273X. PMC 6571867
 . PMID 31100951.
. PMID 31100951.
- ^ "MEROPS Family T1". EMBL-EBI. Diakses tanggal 16 February 2019.
- ^ Nandi D, Tahiliani P, Kumar A, Chandu D (March 2006). "The ubiquitin-proteasome system" (PDF). Journal of Biosciences. 31 (1): 137–55. doi:10.1007/BF02705243. PMID 16595883.
- ^ Heinemeyer W, Fischer M, Krimmer T, Stachon U, Wolf DH (October 1997). "The active sites of the eukaryotic 20 S proteasome and their involvement in subunit precursor processing". The Journal of Biological Chemistry. 272 (40): 25200–9. doi:10.1074/jbc.272.40.25200. PMID 9312134.
- ^ Kumar Deshmukh, Fanindra; Yaffe, Dana; Olshina, Maya; Ben-Nissan, Gili; Sharon, Michal (2019-05-16). "The Contribution of the 20S Proteasome to Proteostasis". Biomolecules (dalam bahasa Inggris). 9 (5): 190. doi:10.3390/biom9050190. ISSN 2218-273X. PMC 6571867
 . PMID 31100951.
. PMID 31100951.
- ^ Nandi D, Tahiliani P, Kumar A, Chandu D (March 2006). "The ubiquitin-proteasome system" (PDF). Journal of Biosciences. 31 (1): 137–55. doi:10.1007/BF02705243. PMID 16595883.
- ^ a b Padmanabhan A, Vuong SA, Hochstrasser M (March 2016). "Assembly of an Evolutionarily Conserved Alternative Proteasome Isoform in Human Cells". Cell Reports. 14 (12): 2962–74. doi:10.1016/j.celrep.2016.02.068. PMC 4828729
 . PMID 26997268.
. PMID 26997268.
- ^ Velichutina I, Connerly PL, Arendt CS, Li X, Hochstrasser M (February 2004). "Plasticity in eucaryotic 20S proteasome ring assembly revealed by a subunit deletion in yeast". The EMBO Journal. 23 (3): 500–10. doi:10.1038/sj.emboj.7600059. PMC 1271798
 . PMID 14739934.
. PMID 14739934.
- ^ Zwickl P, Ng D, Woo KM, Klenk HP, Goldberg AL (September 1999). "An archaebacterial ATPase, homologous to ATPases in the eukaryotic 26 S proteasome, activates protein breakdown by 20 S proteasomes". The Journal of Biological Chemistry. 274 (37): 26008–14. doi:10.1074/jbc.274.37.26008. PMID 10473546.
- ^ Smith DM, Kafri G, Cheng Y, Ng D, Walz T, Goldberg AL (December 2005). "ATP binding to PAN or the 26S ATPases causes association with the 20S proteasome, gate opening, and translocation of unfolded proteins". Molecular Cell. 20 (5): 687–98. doi:10.1016/j.molcel.2005.10.019. PMID 16337593.
- ^ a b Liu CW, Li X, Thompson D, Wooding K, Chang TL, Tang Z, Yu H, Thomas PJ, DeMartino GN (October 2006). "ATP binding and ATP hydrolysis play distinct roles in the function of 26S proteasome". Molecular Cell. 24 (1): 39–50. doi:10.1016/j.molcel.2006.08.025. PMC 3951175
 . PMID 17018291.
. PMID 17018291.
- ^ Lander, Gabriel C.; Estrin, Eric; Matyskiela, Mary E.; Bashore, Charlene; Nogales, Eva; Martin, Andreas (2012-01-11). "Complete subunit architecture of the proteasome regulatory particle". Nature. 482 (7384): 186–191. doi:10.1038/nature10774. ISSN 1476-4687. PMC 3285539
 . PMID 22237024.
. PMID 22237024.
- ^ Lasker, Keren; Förster, Friedrich; Bohn, Stefan; Walzthoeni, Thomas; Villa, Elizabeth; Unverdorben, Pia; Beck, Florian; Aebersold, Ruedi; Sali, Andrej (2012-01-31). "Molecular architecture of the 26S proteasome holocomplex determined by an integrative approach". Proceedings of the National Academy of Sciences of the United States of America. 109 (5): 1380–1387. doi:10.1073/pnas.1120559109. ISSN 1091-6490. PMC 3277140
 . PMID 22307589.
. PMID 22307589.
- ^ Chen, Shuobing; Wu, Jiayi; Lu, Ying; Ma, Yong-Bei; Lee, Byung-Hoon; Yu, Zhou; Ouyang, Qi; Finley, Daniel J.; Kirschner, Marc W. (2016-11-15). "Structural basis for dynamic regulation of the human 26S proteasome". Proceedings of the National Academy of Sciences of the United States of America. 113 (46): 12991–12996. doi:10.1073/pnas.1614614113. ISSN 1091-6490. PMC 5135334
 . PMID 27791164.
. PMID 27791164.
- ^ Chen, Shuobing; Wu, Jiayi; Lu, Ying; Ma, Yong-Bei; Lee, Byung-Hoon; Yu, Zhou; Ouyang, Qi; Finley, Daniel J.; Kirschner, Marc W. (2016-11-15). "Structural basis for dynamic regulation of the human 26S proteasome". Proceedings of the National Academy of Sciences of the United States of America. 113 (46): 12991–12996. doi:10.1073/pnas.1614614113. ISSN 1091-6490. PMC 5135334
 . PMID 27791164.
. PMID 27791164.
- ^ Huang, Xiuliang; Luan, Bai; Wu, Jianping; Shi, Yigong (2016-09). "An atomic structure of the human 26S proteasome". Nature Structural & Molecular Biology (dalam bahasa Inggris). 23 (9): 778–785. doi:10.1038/nsmb.3273. ISSN 1545-9993.
- ^ a b c Zhu Y, Wang WL, Yu D, Ouyang Q, Lu Y, Mao Y (April 2018). "Structural mechanism for nucleotide-driven remodeling of the AAA-ATPase unfoldase in the activated human 26S proteasome". Nature Communications. 9 (1): 1360. Bibcode:2018NatCo...9.1360Z. doi:10.1038/s41467-018-03785-w. PMC 5893597
 . PMID 29636472.
. PMID 29636472.
- ^ a b Unverdorben P, Beck F, Śledź P, Schweitzer A, Pfeifer G, Plitzko JM, Baumeister W, Förster F (April 2014). "Deep classification of a large cryo-EM dataset defines the conformational landscape of the 26S proteasome". Proceedings of the National Academy of Sciences of the United States of America. 111 (15): 5544–9. Bibcode:2014PNAS..111.5544U. doi:10.1073/pnas.1403409111. PMC 3992697
 . PMID 24706844.
. PMID 24706844.
- ^ Beck F, Unverdorben P, Bohn S, Schweitzer A, Pfeifer G, Sakata E, Nickell S, Plitzko JM, Villa E, Baumeister W, Förster F (September 2012). "Near-atomic resolution structural model of the yeast 26S proteasome". Proceedings of the National Academy of Sciences of the United States of America. 109 (37): 14870–5. Bibcode:2012PNAS..10914870B. doi:10.1073/pnas.1213333109. PMC 3443124
 . PMID 22927375.
. PMID 22927375.
- ^ Lander GC, Estrin E, Matyskiela ME, Bashore C, Nogales E, Martin A (February 2012). "Complete subunit architecture of the proteasome regulatory particle". Nature. 482 (7384): 186–91. Bibcode:2012Natur.482..186L. doi:10.1038/nature10774. PMC 3285539
 . PMID 22237024.
. PMID 22237024.
- ^ Chen S, Wu J, Lu Y, Ma YB, Lee BH, Yu Z, Ouyang Q, Finley DJ, Kirschner MW, Mao Y (November 2016). "Structural basis for dynamic regulation of the human 26S proteasome". Proceedings of the National Academy of Sciences of the United States of America. 113 (46): 12991–12996. doi:10.1073/pnas.1614614113. PMC 5135334
 . PMID 27791164.
. PMID 27791164.
- ^ Śledź P, Unverdorben P, Beck F, Pfeifer G, Schweitzer A, Förster F, Baumeister W (April 2013). "Structure of the 26S proteasome with ATP-γS bound provides insights into the mechanism of nucleotide-dependent substrate translocation". Proceedings of the National Academy of Sciences of the United States of America. 110 (18): 7264–7269. Bibcode:2013PNAS..110.7264S. doi:10.1073/pnas.1305782110. PMC 3645540
 . PMID 23589842.
. PMID 23589842.
- ^ Matyskiela ME, Lander GC, Martin A (July 2013). "Conformational switching of the 26S proteasome enables substrate degradation". Nature Structural & Molecular Biology. 20 (7): 781–788. doi:10.1038/nsmb.2616. PMC 3712289
 . PMID 23770819.
. PMID 23770819.
- ^ Lu Y, Wu J, Dong Y, Chen S, Sun S, Ma YB, Ouyang Q, Finley D, Kirschner MW, Mao Y (July 2017). "Conformational Landscape of the p28-Bound Human Proteasome Regulatory Particle". Molecular Cell. 67 (2): 322–333.e6. doi:10.1016/j.molcel.2017.06.007. PMC 5580496
 . PMID 28689658.
. PMID 28689658.
- ^ Köhler A, Cascio P, Leggett DS, Woo KM, Goldberg AL, Finley D (June 2001). "The axial channel of the proteasome core particle is gated by the Rpt2 ATPase and controls both substrate entry and product release". Molecular Cell. 7 (6): 1143–52. doi:10.1016/S1097-2765(01)00274-X. PMID 11430818.
- ^ a b Smith DM, Chang SC, Park S, Finley D, Cheng Y, Goldberg AL (September 2007). "Docking of the proteasomal ATPases' carboxyl termini in the 20S proteasome's alpha ring opens the gate for substrate entry". Molecular Cell. 27 (5): 731–44. doi:10.1016/j.molcel.2007.06.033. PMC 2083707
 . PMID 17803938.
. PMID 17803938.
- ^ Zhu Y, Wang WL, Yu D, Ouyang Q, Lu Y, Mao Y (April 2018). "Structural mechanism for nucleotide-driven remodeling of the AAA-ATPase unfoldase in the activated human 26S proteasome". Nature Communications. 9 (1): 1360. Bibcode:2018NatCo...9.1360Z. doi:10.1038/s41467-018-03785-w. PMC 5893597
 . PMID 29636472.
. PMID 29636472.
- ^ Chen S, Wu J, Lu Y, Ma YB, Lee BH, Yu Z, Ouyang Q, Finley DJ, Kirschner MW, Mao Y (November 2016). "Structural basis for dynamic regulation of the human 26S proteasome". Proceedings of the National Academy of Sciences of the United States of America. 113 (46): 12991–12996. doi:10.1073/pnas.1614614113. PMC 5135334
 . PMID 27791164.
. PMID 27791164.
- ^ Stadtmueller, BM; Hill, CP (7 January 2011). "Proteasome activators". Molecular Cell. 41 (1): 8–19. doi:10.1016/j.molcel.2010.12.020. PMC 3040445
 . PMID 21211719.
. PMID 21211719.
- ^ Förster A, Masters EI, Whitby FG, Robinson H, Hill CP (May 2005). "The 1.9 A structure of a proteasome-11S activator complex and implications for proteasome-PAN/PA700 interactions". Molecular Cell. 18 (5): 589–99. doi:10.1016/j.molcel.2005.04.016. PMID 15916965.
- ^ Wang J, Maldonado MA (August 2006). "The ubiquitin-proteasome system and its role in inflammatory and autoimmune diseases". Cellular & Molecular Immunology. 3 (4): 255–61. PMID 16978533.
- ^ Stadtmueller, BM; Hill, CP (7 January 2011). "Proteasome activators". Molecular Cell. 41 (1): 8–19. doi:10.1016/j.molcel.2010.12.020. PMC 3040445
 . PMID 21211719.
. PMID 21211719.
- ^ Witt S, Kwon YD, Sharon M, Felderer K, Beuttler M, Robinson CV, Baumeister W, Jap BK (July 2006). "Proteasome assembly triggers a switch required for active-site maturation". Structure. 14 (7): 1179–88. doi:10.1016/j.str.2006.05.019. PMID 16843899.
- ^ Xie, Y. (2010-12-01). "Structure, Assembly and Homeostatic Regulation of the 26S Proteasome". Journal of Molecular Cell Biology (dalam bahasa Inggris). 2 (6): 308–317. doi:10.1093/jmcb/mjq030. ISSN 1674-2788.
- ^ Sakata E, Stengel F, Fukunaga K, Zhou M, Saeki Y, Förster F, Baumeister W, Tanaka K, Robinson CV (June 2011). "The catalytic activity of Ubp6 enhances maturation of the proteasomal regulatory particle". Molecular Cell. 42 (5): 637–649. doi:10.1016/j.molcel.2011.04.021. PMID 21658604.
- ^ Bai, Minghui; Zhao, Xian; Sahara, Kazutaka; Ohte, Yuki; Hirano, Yuko; Kaneko, Takeumi; Yashiroda, Hideki; Murata, Shigeo (2019-05-31). "In-depth Analysis of the Lid Subunits Assembly Mechanism in Mammals". Biomolecules (dalam bahasa Inggris). 9 (6): 213. doi:10.3390/biom9060213. ISSN 2218-273X. PMC 6627463
 . PMID 31159305.
. PMID 31159305.
- ^ Haas AL, Warms JV, Hershko A, Rose IA (March 1982). "Ubiquitin-activating enzyme. Mechanism and role in protein-ubiquitin conjugation". The Journal of Biological Chemistry. 257 (5): 2543–8. doi:10.1016/S0021-9258(18)34958-5. PMID 6277905.
- ^ Thrower JS, Hoffman L, Rechsteiner M, Pickart CM (January 2000). "Recognition of the polyubiquitin proteolytic signal". The EMBO Journal. 19 (1): 94–102. doi:10.1093/emboj/19.1.94. PMC 1171781
 . PMID 10619848.
. PMID 10619848.
- ^ Risseeuw EP, Daskalchuk TE, Banks TW, Liu E, Cotelesage J, Hellmann H, Estelle M, Somers DE, Crosby WL (June 2003). "Protein interaction analysis of SCF ubiquitin E3 ligase subunits from Arabidopsis". The Plant Journal. 34 (6): 753–67. doi:10.1046/j.1365-313X.2003.01768.x. PMID 12795696.
- ^ Su, Vivian; Lau, Alan F. (2009-09). "Ubiquitin-like and ubiquitin-associated domain proteins: significance in proteasomal degradation". Cellular and molecular life sciences: CMLS. 66 (17): 2819–2833. doi:10.1007/s00018-009-0048-9. ISSN 1420-9071. PMC 2725189
 . PMID 19468686.
. PMID 19468686.
- ^ Sadanandom A, Bailey M, Ewan R, Lee J, Nelis S (October 2012). "The ubiquitin-proteasome system: central modifier of plant signalling". The New Phytologist. 196 (1): 13–28. doi:10.1111/j.1469-8137.2012.04266.x. PMID 22897362.
- ^ Finley, Daniel; Ulrich, Helle D.; Sommer, Thomas; Kaiser, Peter (2012-10). "The ubiquitin-proteasome system of Saccharomyces cerevisiae". Genetics. 192 (2): 319–360. doi:10.1534/genetics.112.140467. ISSN 1943-2631. PMC 3454868
 . PMID 23028185.
. PMID 23028185.
- ^ Suryadinata, Randy; Roesley, Siti Nur Ain; Yang, George; Sarčević, Boris (2014-07-01). "Mechanisms of generating polyubiquitin chains of different topology". Cells. 3 (3): 674–689. doi:10.3390/cells3030674. ISSN 2073-4409. PMC 4197637
 . PMID 24987835.
. PMID 24987835.
- ^ Li, W.; Ye, Y. (2008-08). "Polyubiquitin chains: functions, structures, and mechanisms". Cellular and molecular life sciences: CMLS. 65 (15): 2397–2406. doi:10.1007/s00018-008-8090-6. ISSN 1420-682X. PMC 2700825
 . PMID 18438605.
. PMID 18438605.
- ^ Xu P, Duong DM, Seyfried NT, Cheng D, Xie Y, Robert J, Rush J, Hochstrasser M, Finley D, Peng J (April 2009). "Quantitative proteomics reveals the function of unconventional ubiquitin chains in proteasomal degradation". Cell. 137 (1): 133–45. doi:10.1016/j.cell.2009.01.041. PMC 2668214
 . PMID 19345192.
. PMID 19345192.
- ^ Akutsu, Masato; Dikic, Ivan; Bremm, Anja (2016-01-01). "Ubiquitin chain diversity at a glance". Journal of Cell Science (dalam bahasa Inggris): jcs.183954. doi:10.1242/jcs.183954. ISSN 1477-9137.
- ^ a b Liu CW, Li X, Thompson D, Wooding K, Chang TL, Tang Z, Yu H, Thomas PJ, DeMartino GN (October 2006). "ATP binding and ATP hydrolysis play distinct roles in the function of 26S proteasome". Molecular Cell. 24 (1): 39–50. doi:10.1016/j.molcel.2006.08.025. PMC 3951175
 . PMID 17018291.
. PMID 17018291.
- ^ Reyes-Turcu, Francisca E.; Ventii, Karen H.; Wilkinson, Keith D. (2009). "Regulation and cellular roles of ubiquitin-specific deubiquitinating enzymes". Annual Review of Biochemistry. 78: 363–397. doi:10.1146/annurev.biochem.78.082307.091526. ISSN 1545-4509. PMC 2734102
 . PMID 19489724.
. PMID 19489724.
- ^ Reyes-Turcu, Francisca E.; Wilkinson, Keith D. (2009-04). "Polyubiquitin binding and disassembly by deubiquitinating enzymes". Chemical Reviews. 109 (4): 1495–1508. doi:10.1021/cr800470j. ISSN 1520-6890. PMC 2734106
 . PMID 19243136.
. PMID 19243136.
- ^ Smith DM, Kafri G, Cheng Y, Ng D, Walz T, Goldberg AL (December 2005). "ATP binding to PAN or the 26S ATPases causes association with the 20S proteasome, gate opening, and translocation of unfolded proteins". Molecular Cell. 20 (5): 687–98. doi:10.1016/j.molcel.2005.10.019. PMID 16337593.
- ^ Majumder, Parijat; Baumeister, Wolfgang (2019-12-18). "Proteasomes: unfoldase-assisted protein degradation machines". Biological Chemistry (dalam bahasa Inggris). 401 (1): 183–199. doi:10.1515/hsz-2019-0344. ISSN 1437-4315.
- ^ Inobe T, Fishbain S, Prakash S, Matouschek A (March 2011). "Defining the geometry of the two-component proteasome degron". Nature Chemical Biology. 7 (3): 161–7. doi:10.1038/nchembio.521. PMC 3129032
 . PMID 21278740.
. PMID 21278740.
- ^ van der Lee R, Lang B, Kruse K, Gsponer J, Sánchez de Groot N, Huynen MA, Matouschek A, Fuxreiter M, Babu MM (September 2014). "Intrinsically disordered segments affect protein half-life in the cell and during evolution". Cell Reports. 8 (6): 1832–44. doi:10.1016/j.celrep.2014.07.055. PMC 4358326
 . PMID 25220455.
. PMID 25220455.
- ^ a b c Smith DM, Kafri G, Cheng Y, Ng D, Walz T, Goldberg AL (December 2005). "ATP binding to PAN or the 26S ATPases causes association with the 20S proteasome, gate opening, and translocation of unfolded proteins". Molecular Cell. 20 (5): 687–98. doi:10.1016/j.molcel.2005.10.019. PMID 16337593.
- ^ Liu CW, Li X, Thompson D, Wooding K, Chang TL, Tang Z, Yu H, Thomas PJ, DeMartino GN (October 2006). "ATP binding and ATP hydrolysis play distinct roles in the function of 26S proteasome". Molecular Cell. 24 (1): 39–50. doi:10.1016/j.molcel.2006.08.025. PMC 3951175
 . PMID 17018291.
. PMID 17018291.
- ^ Hoyt MA, Zich J, Takeuchi J, Zhang M, Govaerts C, Coffino P (April 2006). "Glycine-alanine repeats impair proper substrate unfolding by the proteasome". The EMBO Journal. 25 (8): 1720–9. doi:10.1038/sj.emboj.7601058. PMC 1440830
 . PMID 16601692.
. PMID 16601692.
- ^ a b Zhang M, Coffino P (March 2004). "Repeat sequence of Epstein–Barr virus-encoded nuclear antigen 1 protein interrupts proteasome substrate processing". The Journal of Biological Chemistry. 279 (10): 8635–41. doi:10.1074/jbc.M310449200. PMID 14688254.
- ^ Dick TP, Nussbaum AK, Deeg M, Heinemeyer W, Groll M, Schirle M, Keilholz W, Stevanović S, Wolf DH, Huber R, Rammensee HG, Schild H (October 1998). "Contribution of proteasomal beta-subunits to the cleavage of peptide substrates analyzed with yeast mutants". The Journal of Biological Chemistry. 273 (40): 25637–46. doi:10.1074/jbc.273.40.25637. PMID 9748229.
- ^ Rubin, David M.; Finley, Daniel (1995-08). "Proteolysis: The proteasome: a protein-degrading organelle?". Current Biology (dalam bahasa Inggris). 5 (8): 854–858. doi:10.1016/S0960-9822(95)00172-2.
- ^ Glickman, Michael H.; Ciechanover, Aaron (2002-04-01). "The Ubiquitin-Proteasome Proteolytic Pathway: Destruction for the Sake of Construction". Physiological Reviews (dalam bahasa Inggris). 82 (2): 373–428. doi:10.1152/physrev.00027.2001. ISSN 0031-9333.
- ^ Sahu, Indrajit; Glickman, Michael H. (2021-04-30). "Proteasome in action: substrate degradation by the 26S proteasome". Biochemical Society Transactions (dalam bahasa Inggris). 49 (2): 629–644. doi:10.1042/BST20200382. ISSN 0300-5127.
- ^ Sahu, Indrajit; Glickman, Michael H. (2021-01-24). "Structural Insights into Substrate Recognition and Processing by the 20S Proteasome". Biomolecules (dalam bahasa Inggris). 11 (2): 148. doi:10.3390/biom11020148. ISSN 2218-273X. PMC 7910952
 .
.
- ^ Heinemeyer W, Fischer M, Krimmer T, Stachon U, Wolf DH (October 1997). "The active sites of the eukaryotic 20 S proteasome and their involvement in subunit precursor processing". The Journal of Biological Chemistry. 272 (40): 25200–9. doi:10.1074/jbc.272.40.25200. PMID 9312134.
- ^ Hoppe, Thorsten; Matuschewski, Kai; Rape, Michael; Schlenker, Stephan; Ulrich, Helle D; Jentsch, Stefan (2000-09). "Activation of a Membrane-Bound Transcription Factor by Regulated Ubiquitin/Proteasome-Dependent Processing". Cell (dalam bahasa Inggris). 102 (5): 577–586. doi:10.1016/S0092-8674(00)00080-5.
- ^ Moorthy, Anu K.; Savinova, Olga V.; Ho, Jessica Q.; Wang, Vivien Ya-Fan; Vu, Don; Ghosh, Gourisankar (2006-05-03). "The 20S proteasome processes NF-kappaB1 p105 into p50 in a translation-independent manner". The EMBO journal. 25 (9): 1945–1956. doi:10.1038/sj.emboj.7601081. ISSN 0261-4189. PMC 1456938
 . PMID 16619030.
. PMID 16619030.
- ^ Lata, Sneh; Mishra, Ritu; Banerjea, Akhil C. (2018-11-21). "Proteasomal Degradation Machinery: Favorite Target of HIV-1 Proteins". Frontiers in Microbiology. 9: 2738. doi:10.3389/fmicb.2018.02738. ISSN 1664-302X. PMC 6262318
 . PMID 30524389.
. PMID 30524389.
- ^ Zhang M, Pickart CM, Coffino P (April 2003). "Determinants of proteasome recognition of ornithine decarboxylase, a ubiquitin-independent substrate". The EMBO Journal. 22 (7): 1488–96. doi:10.1093/emboj/cdg158. PMC 152902
 . PMID 12660156.
. PMID 12660156.
- ^ Asher G, Shaul Y (August 2005). "p53 proteasomal degradation: poly-ubiquitination is not the whole story". Cell Cycle. 4 (8): 1015–8. doi:10.4161/cc.4.8.1900. PMID 16082197.
- ^ Shringarpure R, Grune T, Mehlhase J, Davies KJ (January 2003). "Ubiquitin conjugation is not required for the degradation of oxidized proteins by proteasome". The Journal of Biological Chemistry. 278 (1): 311–8. doi:10.1074/jbc.M206279200. PMID 12401807.
- ^ a b c Gille, Christoph; Goede, Andrean; Schlöetelburg, Cord; Preissner, Robert; Kloetzel, Peter Michael; Göbel, Ulf B.; Frömmel, Cornelius (2003-03-07). "A comprehensive view on proteasomal sequences: implications for the evolution of the proteasome". Journal of Molecular Biology. 326 (5): 1437–1448. doi:10.1016/s0022-2836(02)01470-5. ISSN 0022-2836. PMID 12595256.
- ^ Fuchs, Adrian C. D.; Alva, Vikram; Maldoner, Lorena; Albrecht, Reinhard; Hartmann, Marcus D.; Martin, Jörg (2017-06-06). "The Architecture of the Anbu Complex Reflects an Evolutionary Intermediate at the Origin of the Proteasome System". Structure (London, England: 1993). 25 (6): 834–845.e5. doi:10.1016/j.str.2017.04.005. ISSN 1878-4186. PMC 5666114
 . PMID 28479063.
. PMID 28479063.
- ^ Valas, Ruben E.; Bourne, Philip E. (2008-05). "Rethinking proteasome evolution: two novel bacterial proteasomes". Journal of Molecular Evolution. 66 (5): 494–504. doi:10.1007/s00239-008-9075-7. ISSN 0022-2844. PMC 3235984
 . PMID 18389302.
. PMID 18389302.
- ^ Chesnel, Franck; Bazile, Franck; Pascal, Aude; Kubiak, Jacek Z. (2006-08). "Cyclin B dissociation from CDK1 precedes its degradation upon MPF inactivation in mitotic extracts of Xenopus laevis embryos". Cell Cycle (Georgetown, Tex.). 5 (15): 1687–1698. doi:10.4161/cc.5.15.3123. ISSN 1551-4005. PMID 16921258.
- ^ Brito, Daniela A.; Rieder, Conly L. (2006-06-20). "Mitotic checkpoint slippage in humans occurs via cyclin B destruction in the presence of an active checkpoint". Current biology: CB. 16 (12): 1194–1200. doi:10.1016/j.cub.2006.04.043. ISSN 0960-9822. PMC 2749311
 . PMID 16782009.
. PMID 16782009.
- ^ Havens, Courtney G.; Ho, Alan; Yoshioka, Naohisa; Dowdy, Steven F. (2006-06). "Regulation of late G1/S phase transition and APC Cdh1 by reactive oxygen species". Molecular and Cellular Biology. 26 (12): 4701–4711. doi:10.1128/MCB.00303-06. ISSN 0270-7306. PMC 1489138
 . PMID 16738333.
. PMID 16738333.
- ^ Bashir, Tarig; Dorrello, N. Valerio; Amador, Virginia; Guardavaccaro, Daniele; Pagano, Michele (2004-03-11). "Control of the SCF(Skp2-Cks1) ubiquitin ligase by the APC/C(Cdh1) ubiquitin ligase". Nature. 428 (6979): 190–193. doi:10.1038/nature02330. ISSN 1476-4687. PMID 15014502.
- ^ Higashitsuji, Hiroaki; Liu, Yu; Mayer, R. John; Fujita, Jun (2005-10). "The oncoprotein gankyrin negatively regulates both p53 and RB by enhancing proteasomal degradation". Cell Cycle (Georgetown, Tex.). 4 (10): 1335–1337. doi:10.4161/cc.4.10.2107. ISSN 1551-4005. PMID 16177571.
- ^ Tarrason Risa, Gabriel; Hurtig, Fredrik; Bray, Sian; Hafner, Anne E.; Harker-Kirschneck, Lena; Faull, Peter; Davis, Colin; Papatziamou, Dimitra; Mutavchiev, Delyan R. (2020-08-07). "The proteasome controls ESCRT-III-mediated cell division in an archaeon". Science (New York, N.Y.). 369 (6504): eaaz2532. doi:10.1126/science.aaz2532. ISSN 1095-9203. PMC 7116001
 . PMID 32764038.
. PMID 32764038.
- ^ Dharmasiri, Sunethra; Estelle, Mark (2002-06). "The role of regulated protein degradation in auxin response". Plant Molecular Biology. 49 (3-4): 401–409. ISSN 0167-4412. PMID 12036263.
- ^ Weijers, Dolf; Benkova, Eva; Jäger, Katja E.; Schlereth, Alexandra; Hamann, Thorsten; Kientz, Marika; Wilmoth, Jill C.; Reed, Jason W.; Jürgens, Gerd (2005-05-18). "Developmental specificity of auxin response by pairs of ARF and Aux/IAA transcriptional regulators". The EMBO journal. 24 (10): 1874–1885. doi:10.1038/sj.emboj.7600659. ISSN 0261-4189. PMC 1142592
 . PMID 15889151.
. PMID 15889151.
- ^ Haas, A. L.; Baboshina, O.; Williams, B.; Schwartz, L. M. (1995-04-21). "Coordinated induction of the ubiquitin conjugation pathway accompanies the developmentally programmed death of insect skeletal muscle". The Journal of Biological Chemistry. 270 (16): 9407–9412. doi:10.1074/jbc.270.16.9407. ISSN 0021-9258. PMID 7721865.
- ^ Schwartz, L. M.; Kosz, L.; Kay, B. K. (1990-09-01). "Gene activation is required for developmentally programmed cell death". Proceedings of the National Academy of Sciences (dalam bahasa Inggris). 87 (17): 6594–6598. doi:10.1073/pnas.87.17.6594. ISSN 0027-8424. PMC 54583
 . PMID 2395862.
. PMID 2395862.
- ^ Löw, P.; Bussell, K.; Dawson, S. P.; Billett, M. A.; Mayer, R. J.; Reynolds, S. E. (1997-01-06). "Expression of a 26S proteasome ATPase subunit, MS73, in muscles that undergo developmentally programmed cell death, and its control by ecdysteroid hormones in the insect Manduca sexta". FEBS letters. 400 (3): 345–349. doi:10.1016/s0014-5793(96)01413-5. ISSN 0014-5793. PMID 9009228.
- ^ Pitzer, F.; Dantes, A.; Fuchs, T.; Baumeister, W.; Amsterdam, A. (1996-09-23). "Removal of proteasomes from the nucleus and their accumulation in apoptotic blebs during programmed cell death". FEBS letters. 394 (1): 47–50. doi:10.1016/0014-5793(96)00920-9. ISSN 0014-5793. PMID 8925925.
- ^ Orlowski, R. Z. (1999-04). "The role of the ubiquitin-proteasome pathway in apoptosis". Cell Death and Differentiation. 6 (4): 303–313. doi:10.1038/sj.cdd.4400505. ISSN 1350-9047. PMID 10381632.
- ^ Garrido C, Brunet M, Didelot C, Zermati Y, Schmitt E, Kroemer G (November 2006). "Heat shock proteins 27 and 70: anti-apoptotic proteins with tumorigenic properties". Cell Cycle. 5 (22): 2592–601. doi:10.4161/cc.5.22.3448. PMID 17106261.
- ^ Park SH, Bolender N, Eisele F, Kostova Z, Takeuchi J, Coffino P, Wolf DH (January 2007). "The cytoplasmic Hsp70 chaperone machinery subjects misfolded and endoplasmic reticulum import-incompetent proteins to degradation via the ubiquitin-proteasome system". Molecular Biology of the Cell. 18 (1): 153–65. doi:10.1091/mbc.E06-04-0338. PMC 1751312
 . PMID 17065559.
. PMID 17065559.
- ^ Dai Q, Qian SB, Li HH, McDonough H, Borchers C, Huang D, Takayama S, Younger JM, Ren HY, Cyr DM, Patterson C (November 2005). "Regulation of the cytoplasmic quality control protein degradation pathway by BAG2". The Journal of Biological Chemistry. 280 (46): 38673–81. doi:10.1074/jbc.M507986200. PMID 16169850.
- ^ Boguszewska-Mankowska, Dominika; Nykiel, Malgorzata; Zagdanska, Barbara (2015-11-11). Gowder, Sivakumar Joghi Thatha, ed. Protein Oxidation and Redox Regulation of Proteolysis (dalam bahasa Inggris). InTech. doi:10.5772/61182. ISBN 978-953-51-2200-5.
- ^ Shringarpure R, Grune T, Mehlhase J, Davies KJ (January 2003). "Ubiquitin conjugation is not required for the degradation of oxidized proteins by proteasome". The Journal of Biological Chemistry. 278 (1): 311–8. doi:10.1074/jbc.M206279200. PMID 12401807.
- ^ Grune, T.; Shringarpure, R.; Sitte, N.; Davies, K. (2001-11-01). "Age-Related Changes in Protein Oxidation and Proteolysis in Mammalian Cells". The Journals of Gerontology Series A: Biological Sciences and Medical Sciences (dalam bahasa Inggris). 56 (11): B459–B467. doi:10.1093/gerona/56.11.B459. ISSN 1079-5006.
- ^ a b Lehman NL (September 2009). "The ubiquitin proteasome system in neuropathology". Acta Neuropathologica. 118 (3): 329–47. doi:10.1007/s00401-009-0560-x. PMC 2716447
 . PMID 19597829.
. PMID 19597829.
- ^ McNaught KS, Jackson T, JnoBaptiste R, Kapustin A, Olanow CW (May 2006). "Proteasomal dysfunction in sporadic Parkinson's disease". Neurology. 66 (10 Suppl 4): S37–49. doi:10.1212/01.wnl.0000221745.58886.2e. PMID 16717251.
- ^ Zondler, Lisa; Kostka, Marcus; Garidel, Patrick; Heinzelmann, Udo; Hengerer, Bastian; Mayer, Benjamin; Weishaupt, Jochen H.; Gillardon, Frank; Danzer, Karin M. (2017). "Proteasome impairment by α-synuclein". PloS One. 12 (9): e0184040. doi:10.1371/journal.pone.0184040. ISSN 1932-6203. PMC 5612461
 . PMID 28945746.
. PMID 28945746.
- ^ Lecker, Stewart H.; Goldberg, Alfred L.; Mitch, William E. (2006-07). "Protein Degradation by the Ubiquitin–Proteasome Pathway in Normal and Disease States". Journal of the American Society of Nephrology (dalam bahasa Inggris). 17 (7): 1807–1819. doi:10.1681/ASN.2006010083. ISSN 1046-6673.
- ^ Wang J, Maldonado MA (August 2006). "The ubiquitin-proteasome system and its role in inflammatory and autoimmune diseases". Cellular & Molecular Immunology. 3 (4): 255–61. PMID 16978533.
- ^ Murata, Shigeo; Sasaki, Katsuhiro; Kishimoto, Toshihiko; Niwa, Shin-ichiro; Hayashi, Hidemi; Takahama, Yousuke; Tanaka, Keiji (2007-06). "Regulation of CD8 + T Cell Development by Thymus-Specific Proteasomes". Science (dalam bahasa Inggris). 316 (5829): 1349–1353. doi:10.1126/science.1141915. ISSN 0036-8075.
- ^ Cascio P, Hilton C, Kisselev AF, Rock KL, Goldberg AL (May 2001). "26S proteasomes and immunoproteasomes produce mainly N-extended versions of an antigenic peptide". The EMBO Journal. 20 (10): 2357–66. doi:10.1093/emboj/20.10.2357. PMC 125470
 . PMID 11350924.
. PMID 11350924.
- ^ Wang J, Maldonado MA (August 2006). "The ubiquitin-proteasome system and its role in inflammatory and autoimmune diseases". Cellular & Molecular Immunology. 3 (4): 255–61. PMID 16978533.
- ^ Mallery DL, McEwan WA, Bidgood SR, Towers GJ, Johnson CM, James LC (November 2010). "Antibodies mediate intracellular immunity through tripartite motif-containing 21 (TRIM21)". Proceedings of the National Academy of Sciences of the United States of America. 107 (46): 19985–19990. Bibcode:2010PNAS..10719985M. doi:10.1073/pnas.1014074107. PMC 2993423
 . PMID 21045130.
. PMID 21045130.
- ^ Kleiger, Gary; Mayor, Thibault (2014-06). "Perilous journey: a tour of the ubiquitin-proteasome system". Trends in Cell Biology. 24 (6): 352–359. doi:10.1016/j.tcb.2013.12.003. ISSN 1879-3088. PMC 4037451
 . PMID 24457024.
. PMID 24457024.
- ^ Goldberg, A. L.; Stein, R.; Adams, J. (1995-08). "New insights into proteasome function: from archaebacteria to drug development". Chemistry & Biology. 2 (8): 503–508. doi:10.1016/1074-5521(95)90182-5. ISSN 1074-5521. PMID 9383453.
- ^ Penke, Botond; Bogár, Ferenc; Fülöp, Lívia (2017-10-10). "β-Amyloid and the Pathomechanisms of Alzheimer's Disease: A Comprehensive View". Molecules (dalam bahasa Inggris). 22 (10): 1692. doi:10.3390/molecules22101692. ISSN 1420-3049. PMC 6151811
 . PMID 28994715.
. PMID 28994715.
- ^ Ortega, Zaira; Lucas, Jose J. (2014). "Ubiquitin-proteasome system involvement in Huntington's disease". Frontiers in Molecular Neuroscience. 7: 77. doi:10.3389/fnmol.2014.00077. ISSN 1662-5099. PMC 4179678
 . PMID 25324717.
. PMID 25324717.
- ^ Sandri, Marco; Robbins, Jeffrey (2014-06). "Proteotoxicity: an underappreciated pathology in cardiac disease". Journal of Molecular and Cellular Cardiology. 71: 3–10. doi:10.1016/j.yjmcc.2013.12.015. ISSN 1095-8584. PMC 4011959
 . PMID 24380730.
. PMID 24380730.
- ^ Wang, Zhao V.; Hill, Joseph A. (2015-02-03). "Protein quality control and metabolism: bidirectional control in the heart". Cell Metabolism. 21 (2): 215–226. doi:10.1016/j.cmet.2015.01.016. ISSN 1932-7420. PMC 4317573
 . PMID 25651176.
. PMID 25651176.
- ^ a b Hoesel, Bastian; Schmid, Johannes A (2013). "The complexity of NF-κB signaling in inflammation and cancer". Molecular Cancer (dalam bahasa Inggris). 12 (1): 86. doi:10.1186/1476-4598-12-86. ISSN 1476-4598. PMC 3750319
 . PMID 23915189.
. PMID 23915189.
- ^ Liu, Ting; Zhang, Lingyun; Joo, Donghyun; Sun, Shao-Cong (2017-12). "NF-κB signaling in inflammation". Signal Transduction and Targeted Therapy (dalam bahasa Inggris). 2 (1): 17023. doi:10.1038/sigtrans.2017.23. ISSN 2059-3635. PMC 5661633
 . PMID 29158945.
. PMID 29158945.
- ^ Ermolaeva, Maria A.; Dakhovnik, Alexander; Schumacher, Björn (2015-09). "Quality control mechanisms in cellular and systemic DNA damage responses". Ageing Research Reviews. 23 (Pt A): 3–11. doi:10.1016/j.arr.2014.12.009. ISSN 1872-9649. PMC 4886828
 . PMID 25560147.
. PMID 25560147.
- ^ Checler, F.; da Costa, C. A.; Ancolio, K.; Chevallier, N.; Lopez-Perez, E.; Marambaud, P. (2000-07-26). "Role of the proteasome in Alzheimer's disease". Biochimica Et Biophysica Acta. 1502 (1): 133–138. doi:10.1016/s0925-4439(00)00039-9. ISSN 0006-3002. PMID 10899438.
- ^ Zheng, Qiuyang; Huang, Timothy; Zhang, Lishan; Zhou, Ying; Luo, Hong; Xu, Huaxi; Wang, Xin (2016-12-15). "Dysregulation of Ubiquitin-Proteasome System in Neurodegenerative Diseases". Frontiers in Aging Neuroscience. 8. doi:10.3389/fnagi.2016.00303. ISSN 1663-4365. PMC 5156861
 . PMID 28018215.
. PMID 28018215.
- ^ a b c Jansen, Anne H. P.; Reits, Eric A. J.; Hol, Elly M. (2014-08-08). "The ubiquitin proteasome system in glia and its role in neurodegenerative diseases". Frontiers in Molecular Neuroscience. 7. doi:10.3389/fnmol.2014.00073. ISSN 1662-5099. PMC 4126450
 . PMID 25152710.
. PMID 25152710.
- ^ Opattova, Alena; Cente, Martin; Novak, Michal; Filipcik, Peter (2015-10). "The ubiquitin proteasome system as a potential therapeutic target for treatment of neurodegenerative diseases". General Physiology and Biophysics. 34 (4): 337–352. doi:10.4149/gpb_2015024. ISSN 0231-5882. PMID 26221742.
- ^ Deriziotis, Pelagia; Tabrizi, Sarah J. (2008-12). "Prions and the proteasome". Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease (dalam bahasa Inggris). 1782 (12): 713–722. doi:10.1016/j.bbadis.2008.06.011.
- ^ Zhu, Ting; Hayat Khan, Sher; Zhao, Deming; Yang, Lifeng (2014-07). "Regulation of proteasomes in prion disease". Acta Biochimica et Biophysica Sinica (dalam bahasa Inggris). 46 (7): 531–539. doi:10.1093/abbs/gmu031. ISSN 1745-7270.
- ^ Calise, Justine; Powell, Saul R. (2013-02-01). "The ubiquitin proteasome system and myocardial ischemia". American Journal of Physiology. Heart and Circulatory Physiology. 304 (3): H337–349. doi:10.1152/ajpheart.00604.2012. ISSN 1522-1539. PMC 3774499
 . PMID 23220331.
. PMID 23220331.
- ^ Predmore, Jaime M.; Wang, Ping; Davis, Frank; Bartolone, Sarah; Westfall, Margaret V.; Dyke, David B.; Pagani, Francis; Powell, Saul R.; Day, Sharlene M. (2010-03-02). "Ubiquitin proteasome dysfunction in human hypertrophic and dilated cardiomyopathies". Circulation. 121 (8): 997–1004. doi:10.1161/CIRCULATIONAHA.109.904557. ISSN 1524-4539. PMC 2857348
 . PMID 20159828.
. PMID 20159828.
- ^ Powell, Saul R. (2006-07). "The ubiquitin-proteasome system in cardiac physiology and pathology". American Journal of Physiology. Heart and Circulatory Physiology. 291 (1): H1–H19. doi:10.1152/ajpheart.00062.2006. ISSN 0363-6135. PMID 16501026.
- ^ Almond, Jb; Cohen, Gm (2002-04). "The proteasome: a novel target for cancer chemotherapy". Leukemia (dalam bahasa Inggris). 16 (4): 433–443. doi:10.1038/sj.leu.2402417. ISSN 0887-6924.
- ^ Bunn, Paul A. (2004-06-15). "The Potential Role of Proteasome Inhibitors in the Treatment of Lung Cancer". Clinical Cancer Research (dalam bahasa Inggris). 10 (12): 4263s–4265s. doi:10.1158/1078-0432.CCR-040011. ISSN 1078-0432.
- ^ Zhu, Bo; Zhu, Lihua; Xia, Lin; Xiong, Yuyun; Yin, Qing; Rui, Ke (2020-11-16). "Roles of Ubiquitination and Deubiquitination in Regulating Dendritic Cell Maturation and Function". Frontiers in Immunology. 11: 586613. doi:10.3389/fimmu.2020.586613. ISSN 1664-3224. PMC 7717991
 .
.
- ^ Egerer, Karl; Kuckelkorn, Ulrike; Rudolph, Paul E.; Rückert, Jens C.; Dörner, Thomas; Burmester, Gerd-R.; Kloetzel, Peter-M.; Feist, Eugen (2002-10). "Circulating proteasomes are markers of cell damage and immunologic activity in autoimmune diseases". The Journal of Rheumatology. 29 (10): 2045–2052. ISSN 0315-162X. PMID 12375310.
- ^ Ōmura, Satoshi; Crump, Andy (2019-04). "Lactacystin: first-in-class proteasome inhibitor still excelling and an exemplar for future antibiotic research". The Journal of Antibiotics (dalam bahasa Inggris). 72 (4): 189–201. doi:10.1038/s41429-019-0141-8. ISSN 0021-8820. PMC 6760633
 . PMID 30755736.
. PMID 30755736.
- ^ Roeten, Margot S. F.; Cloos, Jacqueline; Jansen, Gerrit (2018-02). "Positioning of proteasome inhibitors in therapy of solid malignancies". Cancer Chemotherapy and Pharmacology (dalam bahasa Inggris). 81 (2): 227–243. doi:10.1007/s00280-017-3489-0. ISSN 0344-5704. PMC 5778165
 . PMID 29184971.
. PMID 29184971.
- ^ Richardson, Paul G.; Mitsiades, Constantine; Hideshima, Teru; Anderson, Kenneth C. (2005-02-19). "Proteasome Inhibition in the Treatment of Cancer". Cell Cycle (dalam bahasa Inggris). 4 (2): 289–295. doi:10.4161/cc.4.2.1414. ISSN 1538-4101.
- ^ Fisher, Richard I.; Bernstein, Steven H.; Kahl, Brad S.; Djulbegovic, Benjamin; Robertson, Michael J.; de Vos, Sven; Epner, Elliot; Krishnan, Amrita; Leonard, John P. (2006-10-20). "Multicenter phase II study of bortezomib in patients with relapsed or refractory mantle cell lymphoma". Journal of Clinical Oncology: Official Journal of the American Society of Clinical Oncology. 24 (30): 4867–4874. doi:10.1200/JCO.2006.07.9665. ISSN 1527-7755. PMID 17001068.
- ^ Jakob, Christian; Egerer, Karl; Liebisch, Peter; Türkmen, Seval; Zavrski, Ivana; Kuckelkorn, Ulrike; Heider, Ulrike; Kaiser, Martin; Fleissner, Claudia (2007-03-01). "Circulating proteasome levels are an independent prognostic factor for survival in multiple myeloma". Blood. 109 (5): 2100–2105. doi:10.1182/blood-2006-04-016360. ISSN 0006-4971. PMID 17095627.
- ^ Shah, S. A.; Potter, M. W.; McDade, T. P.; Ricciardi, R.; Perugini, R. A.; Elliott, P. J.; Adams, J.; Callery, M. P. (2001 Apr 2-27). "26S proteasome inhibition induces apoptosis and limits growth of human pancreatic cancer". Journal of Cellular Biochemistry. 82 (1): 110–122. doi:10.1002/jcb.1150. ISSN 0730-2312. PMID 11400168.
- ^ Liu, Wei; Chen, Juan; Tamayo, Archito T.; Ruan, Changgeng; Li, Li; Zhou, Shouhao; Shen, Chan; Young, Ken H.; Westin, Jason (2018-01-02). "Preclinical efficacy and biological effects of the oral proteasome inhibitor ixazomib in diffuse large B-cell lymphoma". Oncotarget (dalam bahasa Inggris). 9 (1): 346–360. doi:10.18632/oncotarget.20378. ISSN 1949-2553. PMC 5787470
 . PMID 29416618.
. PMID 29416618.
- ^ O'Connor, Owen A.; Wright, John; Moskowitz, Craig; Muzzy, Jamie; MacGregor-Cortelli, Barbara; Stubblefield, Michael; Straus, David; Portlock, Carol; Hamlin, Paul (2005-02-01). "Phase II clinical experience with the novel proteasome inhibitor bortezomib in patients with indolent non-Hodgkin's lymphoma and mantle cell lymphoma". Journal of Clinical Oncology: Official Journal of the American Society of Clinical Oncology. 23 (4): 676–684. doi:10.1200/JCO.2005.02.050. ISSN 0732-183X. PMID 15613699.
- ^ Mato, Anthony R.; Feldman, Tatyana; Goy, André (2012-05-01). "Proteasome Inhibition and Combination Therapy for Non-Hodgkin's Lymphoma: From Bench to Bedside". The Oncologist (dalam bahasa Inggris). 17 (5): 694–707. doi:10.1634/theoncologist.2011-0341. ISSN 1083-7159. PMC 3360909
 . PMID 22566373.
. PMID 22566373.
- ^ Messinger, Yoav H.; Gaynon, Paul S.; Sposto, Richard; van der Giessen, Jeannette; Eckroth, Elena; Malvar, Jemily; Bostrom, Bruce C.; Therapeutic Advances in Childhood Leukemia & Lymphoma (TACL) Consortium (2012-07-12). "Bortezomib with chemotherapy is highly active in advanced B-precursor acute lymphoblastic leukemia: Therapeutic Advances in Childhood Leukemia & Lymphoma (TACL) Study". Blood. 120 (2): 285–290. doi:10.1182/blood-2012-04-418640. ISSN 1528-0020. PMID 22653976.
- ^ Pufall, Miles A. (2015). "Glucocorticoids and Cancer". Advances in Experimental Medicine and Biology. 872: 315–333. doi:10.1007/978-1-4939-2895-8_14. ISSN 0065-2598. PMC 5546099
 . PMID 26216001.
. PMID 26216001.
- ^ Schmidtke, G.; Holzhütter, H. G.; Bogyo, M.; Kairies, N.; Groll, M.; de Giuli, R.; Emch, S.; Groettrup, M. (1999-12-10). "How an inhibitor of the HIV-I protease modulates proteasome activity". The Journal of Biological Chemistry. 274 (50): 35734–35740. doi:10.1074/jbc.274.50.35734. ISSN 0021-9258. PMID 10585454.
- ^ Laurent, Nathalie; de Boüard, Sophie; Guillamo, Jean-Sébastien; Christov, Christo; Zini, Roland; Jouault, Hélène; Andre, Patrice; Lotteau, Vincent; Peschanski, Marc (2004-02). "Effects of the proteasome inhibitor ritonavir on glioma growth in vitro and in vivo". Molecular Cancer Therapeutics. 3 (2): 129–136. ISSN 1535-7163. PMID 14985453.
- ^ Zollner, Thomas M.; Podda, Maurizio; Pien, Christine; Elliott, Peter J.; Kaufmann, Roland; Boehncke, Wolf-Henning (2002-03). "Proteasome inhibition reduces superantigen-mediated T cell activation and the severity of psoriasis in a SCID-hu model". The Journal of Clinical Investigation. 109 (5): 671–679. doi:10.1172/JCI12736. ISSN 0021-9738. PMC 150886
 . PMID 11877475.
. PMID 11877475.
- ^ Elliott, P. J.; Pien, C. S.; McCormack, T. A.; Chapman, I. D.; Adams, J. (1999-08). "Proteasome inhibition: A novel mechanism to combat asthma". The Journal of Allergy and Clinical Immunology. 104 (2 Pt 1): 294–300. doi:10.1016/s0091-6749(99)70369-6. ISSN 0091-6749. PMID 10452747.
- ^ Hubbell, Grace E.; Tepe, Jetze J. (2020). "Natural product scaffolds as inspiration for the design and synthesis of 20S human proteasome inhibitors". RSC Chemical Biology (dalam bahasa Inggris). 1 (5): 305–332. doi:10.1039/D0CB00111B. ISSN 2633-0679.
- ^ Verdoes, Martijn; Florea, Bogdan I.; Menendez-Benito, Victoria; Maynard, Christa J.; Witte, Martin D.; van der Linden, Wouter A.; van den Nieuwendijk, Adrianus M. C. H.; Hofmann, Tanja; Berkers, Celia R. (2006-11). "A fluorescent broad-spectrum proteasome inhibitor for labeling proteasomes in vitro and in vivo". Chemistry & Biology. 13 (11): 1217–1226. doi:10.1016/j.chembiol.2006.09.013. ISSN 1074-5521. PMID 17114003.
