Hidrosililasi
Hidrosililasi, juga disebut hidrosilasi katalitik, menjelaskan penambahan ikatan Si-H pada ikatan tak jenuh.[1] Biasanya reaksi dilakukan secara katalitik dan biasanya substratnya adalah senyawa organik tak jenuh. Alkena dan alkuna menghasilkan alkil dan vinilsilan; aldehida dan keton menghasilkan silil eter. Hidrosililasi telah disebut sebagai "aplikasi paling penting dari platina dalam katalisis homogen."[2]
Ruang lingkup dan mekanisme[sunting | sunting sumber]
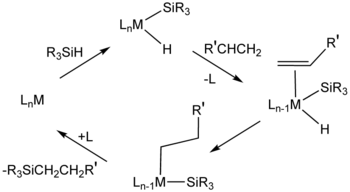
Hidrosililasi alkena merupakan metode yang penting secara komersial untuk membuat senyawa organosilikon. Proses ini secara mekanis mirip dengan hidrogenasi alkena. Bahkan, katalis serupa kadang-kadang digunakan untuk dua proses katalitik.
Mekanisme umum, yang disebut mekanisme Chalk-Harrod, mengasumsikan kompleks logam antara yang mengandung hidrida, ligan silil (R3Si), dan substrat alkena. Adisi oksidatif berlangsung melalui intermediasi kompleks sigma, di mana ikatan Si-H tidak sepenuhnya putus.
Hidrosililasi alkena biasanya berlangsung melalui adisi anti-Markovnikov, yaitu, silikon ditempatkan pada karbon terminal ketika penghidrosililasian sebuah variasi alkena terminal[1] dari mekanisme Chalk-Harrod. Beberapa kasus melibatkan penyisipan alkena ke dalam ikatan M-Si diikuti oleh eliminasi reduktif, kebalikan dari urutan dalam mekanisme Chalk-Harrod. Dalam kasus tertentu, hidrosililasi menghasilkan vinil atau silan alilik yang dihasilkan dari eliminasi hidrida beta.[3]
Alkuna juga mengalami hidrosililasi, misalnya, penambahan trietilsilan ke difenilasetilen:[4]
- Et3SiH + PhC≡CPh → Et3Si(Ph)C=CH(Ph)
Hidrosililasi asimetris[sunting | sunting sumber]
Menggunakan fosfin kiral sebagai ligan spektator, katalis telah dikembangkan untuk hidrosilasi asimetris katalitik. Reaksi yang dipelajari dengan baik adalah penambahan triklorosilan ke stirena untuk menghasilkan 1-fenil-1-(triklorosilil)etana:
- Cl3SiH + PhCH=CH2 → (Ph)(CH3)CHSiCl3
Enantioselektivitas yang hampir sempurna dapat dicapai dengan menggunakan katalis paladium yang didukung oleh ligan monofosfin yang tersubstitusi binaftil.[5]
Hidrosililasi permukaan[sunting | sunting sumber]
Wafer silikon dapat digores dalam asam fluorida (HF) untuk menghilangkan oksida asli dan membentuk permukaan silikon yang diakhiri hidrogen. Permukaan yang diakhiri hidrogen mengalami hidrosilasi dengan senyawa tak jenuh (seperti alkena dan alkuna terminal), untuk membentuk lapisan tunggal yang stabil pada permukaan. Sebagai contoh:
- Si-H + H2C=CH(CH2)7CH3 → Si-CH2CHH-(CH2)7CH3
Reaksi hidrosililasi dapat dimulai dengan sinar UV pada suhu kamar atau dengan panas (suhu reaksi khas 120-200 °C), di bawah kondisi bebas uap air dan oksigen.[6] Lapisan tunggal yang dihasilkan, yang stabil dan lengai, menghambat oksidasi lapisan silikon dasar, yang relevan dengan berbagai aplikasi perangkat.[7]
Katalis[sunting | sunting sumber]

Sebelum pengenalan katalis platina oleh Speier, hidrosililasi tidak dipraktekkan secara luas. Proses katalis peroksida dilaporkan dalam literatur akademis pada tahun 1947,[8] tetapi pengenalan katalis Speier (H2PtCl6) merupakan terobosan besar.
Katalis Karstedt kemudian diperkenalkan. Katalis ini merupakan kompleks lipofilik yang larut dalam substrat organik bagi kepentingan industri.[9] Kompleks dan senyawa yang mengkatalisis hidrogenasi seringkali merupakan katalis yang efektif untuk hidrosililasi, misalnya katalis Wilkinson.
Referensi[sunting | sunting sumber]
- ^ a b "Hydrosilylation A Comprehensive Review on Recent Advances" B. Marciniec (ed.), Advances in Silicon Science, Springer Science, 2009. doi:10.1007/978-1-4020-8172-9
- ^ Renner, H.; Schlamp, G.; Kleinwächter, I.; Drost, E.; Lüschow, H. M.; Tews, P.; Panster, P.; Diehl, M.; Lang, J.; Kreuzer, T.; Knödler, A.; Starz, K. A.; Dermann, K.; Rothaut, J.; Drieselman, R. (2002). "Platinum group metals and compounds". Ullmann's Encyclopedia of Industrial Chemistry. Wiley. doi:10.1002/14356007.a21_075.
- ^ Troegel, D.; Stohrer, J. (2011). "Recent Advances and Actual Challenges in Late Transition Metal Catalyzed Hydrosilylation of Olefins from an Industrial Point of View". Coord. Chem. Rev. 255: 1440–1459. doi:10.1016/j.ccr.2010.12.025.
- ^ James L. Fry, Ronald J. Rahaim Jr., Robert E. Maleczka, Jr. "Triethylsilane", Encyclopedia of Reagents for Organic Synthesis, John Wiley & Sons, 2007. DOI:10.1002/047084289X.rt226.pub2
- ^ Hayashi, T.; Yamasaki, K. (2007). "C–E Bond Formation through Asymmetric Hydrosilylation of Alkenes". Dalam Crabtree, Robert H.; D. Michael P. Mingos. Comprehensive Organometallic Chemistry III. Amsterdam: Elsevier. doi:10.1016/B0-08-045047-4/00140-0. ISBN 978-0-08-045047-6.
- ^ "Photoreactivity of Unsaturated Compounds with Hydrogen-Terminated Silicon (111)," R. L. Cicero, M. R. Linford, C. E. D. Chidsey, Langmuir 16, 5688-5695 (2000)
- ^ Direct electrical detection of DNA Hybridization at DNA-modified silicon surfaces, W.Cai, J. Peck, D. van der Weide, and R.J. Hamers, Biosensors and Bioelectronics 19, 1013-1019 (2004)
- ^ Sommer, L.; Pietrusza, E.; Whitmore, F. "Peroxide-catalyzed addition of trichlorosilane to 1-octene". J. Am. Chem. Soc. 69 (1): 188. doi:10.1021/ja01193a508.
- ^ C. Elschenbroich, Organometallics (2006) Wiley and Sons-VCH: Weinheim. ISBN 978-3-527-29390-2
Bacaan lebih lanjut[sunting | sunting sumber]
Buku
- Applied homogeneous catalysis with organometallic compounds : a comprehensive handbook : applications, developments. Boy Cornils; W A Herrmann. Publisher: Weinheim ; New York : Wiley-VCH, 2000.
- Comprehensive handbook on hydrosilylation. Bogdan Marciniec. Publisher: Oxford [u.a.] : Pergamon Press, 1992.
- Rhodium complexes as hydrosilylation catalysts. N.K. Skvortsov. // Rhodium Express. 1994. No 4 (May). P. 3 - 36 (Eng). [1] Diarsipkan 2022-06-23 di Wayback Machine. ISSN 0869-7876
Artikel
- "Alkyl Monolayers on Silicon Prepared from 1-Alkenes and Hydrogen-Terminated Silicon," M. R. Linford, P. Fenter, P. M. Eisenberger and C. E. D. Chidsey, J. Am. Chem. Soc. 117, 3145-3155 (1995).
- "Synthesis and characterization of DNA-modified Si(111) Surfaces," T. Strother, W. CAi, X. Zhao, R.J. Hamers, and L.M. Smith, J. Am. Chem. Soc. 122, 1205-1209 (2000).
- "T. Strother, R.J. Hamers, and L.M. Smith, "Surface Chemistry of DNA Covalent Attachment to the Silicon(100) Surface". Langmuir, 2002, 18, 788-796.
- "Covalently Modified Silicon and Diamond Surfaces: Resistance to Non-Specific Protein Adsorption and Optimization for Biosensing," T.L. Lasseter, B.H. Clare, N.L. Abbott, and R.J. Hamers. J. Am. Chem. Soc. 2004, 126, 10220-10221.
